题目内容
16.在较高温度下的某溶液中,硝酸钾、氯化钠均达饱和,冷却析出晶体的成分是( )| A. | 纯硝酸钾晶体 | B. | 大量硝酸钾晶体,少量氯化钠 | ||
| C. | 等量的硝酸钾和氯化钠 | D. | 大量氯化钠,少量硝酸钾 |
分析 不同物质的溶解度受温度变化影响不同,硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度随温度升高而升高,但受温度变化影响不大.在冷却热饱和溶液时硝酸钾容易析出晶体,氯化钠析出较少.
解答 解:不同物质的溶解度受温度变化影响不同,硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度随温度升高而升高,但受温度变化影响不大.在冷却热饱和溶液时硝酸钾容易析出晶体,氯化钠析出较少,所以冷却析出晶体的成分大量硝酸钾晶体,少量氯化钠,故B正确.
故选B.
点评 本题主要考查温度对溶解度的影响,硝酸钾的溶解度随温度升高而升高,氯化钠的溶解度随温度变化比较小,熟石灰的溶解度随温度的升高而降低.要求学生熟练掌握一些常见物质的溶解度受温度的影响,题目难度不大.

练习册系列答案
相关题目
6. 某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL,H2C2O4溶液(0.1mol•L-1 )的用量均为2mL.
某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL,H2C2O4溶液(0.1mol•L-1 )的用量均为2mL.
(1)该反应的离子方程式:2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O.
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
(3)在完成探究催化剂对该反应速率影响的实验时发现,未加催化剂的情况下,刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.
针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是生成的Mn2+催化反应的进行.若用实验证明你的猜想.除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是B.
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(4)可以利用酸性高锰酸钾测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数.该小组称量2.68g草酸钠样品溶于稀硫酸中,然后用0.2000mol•L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应 ).
①滴定前是否要滴加指示剂?否(填“是”或“否”),当溶液由无色变为紫红色,且在半分钟内不褪色,说明滴定达到终点.
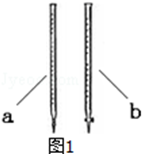
②滴定时用b(填a或b )滴定管盛装KMnO4标准溶液.
③达到终点时消耗了15.00mL的高锰酸钾溶液,样品中草酸钠的质量分数为37.5%.
 某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL,H2C2O4溶液(0.1mol•L-1 )的用量均为2mL.
某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL,H2C2O4溶液(0.1mol•L-1 )的用量均为2mL.(1)该反应的离子方程式:2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O.
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂的用量/g | KMnO4酸性溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究催化剂对该反应速率的影响 |
| ② | ||||
| ③ | ||||
| ④ |
针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是生成的Mn2+催化反应的进行.若用实验证明你的猜想.除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是B.
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(4)可以利用酸性高锰酸钾测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数.该小组称量2.68g草酸钠样品溶于稀硫酸中,然后用0.2000mol•L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应 ).
①滴定前是否要滴加指示剂?否(填“是”或“否”),当溶液由无色变为紫红色,且在半分钟内不褪色,说明滴定达到终点.
②滴定时用b(填a或b )滴定管盛装KMnO4标准溶液.
③达到终点时消耗了15.00mL的高锰酸钾溶液,样品中草酸钠的质量分数为37.5%.
7.针对实验室制取氨气,下列说法不正确的是( )
| A. | 发生装置与氯酸钾制取氧气相同 | |
| B. | 可以用碱石灰干燥氨气 | |
| C. | 棉花的作用和高锰酸钾制取氧气一样 | |
| D. | 氨气验满的方法是将湿润的红色石蕊试纸放于集气瓶附近 |
4.在①浓盐酸 ②氧气 ③浓硫酸 ④氢氟酸 ⑤氢氧化钾溶液中,能与单质硅起化学反应的是( )
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②④⑤ |
11.下列实验操作中正确的是( )
| A. | 苯的硝化反应中,向浓硫酸中加浓硝酸制得混合酸 | |
| B. | 向稀氨水中逐渐加入硝酸银溶液来配制银氨溶液 | |
| C. | 向相对过量的氢氧化钠溶液中滴入少量硫酸铜溶液以配制新制氢氧化铜 | |
| D. | 溴乙烷在氢氧化钠溶液的存在下进行水解后,加入硝酸银溶液,可检验溴离子的存在 |
1.某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了如图1实验流程图:

请回答以下问题:
(1)为验证气体A,按图2所示进行实验:若能观察到KMnO4溶液(紫红色)褪色的现象,即可证明火柴头上含有S元素.
(2)要证明火柴头中含有Cl元素的后续实验步骤是取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素.
(3)有学生提出检验火柴头上KClO3另一套实验方案:(如图3)
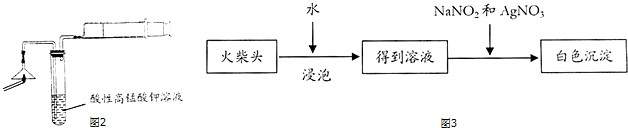
有关的离子反应方程式为ClO3-+3NO2-+Ag+=AgCl↓+3NO3-,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是二氧化锰和浓盐酸加热也发生反应生成氯气.
(4)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验.
由上表可知,实验①和⑤能证明温度越高,化学反应速率越快,实验②和③,证明物质D的用量越大,反应速率越快.
(5)写出步骤①中发生反应的两个化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.

请回答以下问题:
(1)为验证气体A,按图2所示进行实验:若能观察到KMnO4溶液(紫红色)褪色的现象,即可证明火柴头上含有S元素.
(2)要证明火柴头中含有Cl元素的后续实验步骤是取滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素.
(3)有学生提出检验火柴头上KClO3另一套实验方案:(如图3)

有关的离子反应方程式为ClO3-+3NO2-+Ag+=AgCl↓+3NO3-,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是二氧化锰和浓盐酸加热也发生反应生成氯气.
(4)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验.
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
(5)写出步骤①中发生反应的两个化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
8.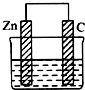 一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
锌片:2Zn-4e-+4OH-═2ZnO+2H2O
石墨:2H2O+O2+4e-═4OH-
下列说法中不正确的是( )
 一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:锌片:2Zn-4e-+4OH-═2ZnO+2H2O
石墨:2H2O+O2+4e-═4OH-
下列说法中不正确的是( )
| A. | 电子从石墨经外电路流向锌片,电解质溶液为酸性溶液 | |
| B. | 锌片是负极,石墨是正极 | |
| C. | 电池总反应为2Zn+O2═2ZnO | |
| D. | 该原电池工作一段时间后石墨附近溶液中的c(OH-)增大 |
5.下列分子中所有原子都满足最外层8电子结构的是( )
| A. | NH3 | B. | PCl5 | C. | CO2 | D. | CO(NH2)2 |
6.下列物质的转化中,浓HNO3既表现了氧化性,又表现了酸性的是( )
| A. | Cu→Cu(NO3)2 | B. | C→CO2 | C. | CuO→Cu(NO3)2 | D. | Fe2O3→Fe(NO3)3 |