题目内容
17.下列说法不正确的是( )| A. | 使用催化剂,可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强正反应速率和逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
分析 化学反应中,影响化学反应速率的主要因素为物质的性质,催化剂具有选择性,对于气体参加的反应,增大压强,升高温度,可增大反应速率,反之降低反应速率.
解答 解:A.使用催化剂,正逆反应速率都加快,故A正确;
B.可逆反应A(g)?B(g)+C(g),增大压强,正逆反应速率都增大,故B正确;
C.降低温度,正逆反应速率都减小,故C错误;
D.化学反应中,影响化学反应速率的主要因素为物质的性质,故D正确;
故选C.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重双基的考查,题目难度中等,注意相关基础知识的学习,为解答该类题目的前提.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案
相关题目
7.针对实验室制取氨气,下列说法不正确的是( )
| A. | 发生装置与氯酸钾制取氧气相同 | |
| B. | 可以用碱石灰干燥氨气 | |
| C. | 棉花的作用和高锰酸钾制取氧气一样 | |
| D. | 氨气验满的方法是将湿润的红色石蕊试纸放于集气瓶附近 |
8.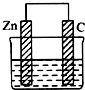 一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
锌片:2Zn-4e-+4OH-═2ZnO+2H2O
石墨:2H2O+O2+4e-═4OH-
下列说法中不正确的是( )
 一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:锌片:2Zn-4e-+4OH-═2ZnO+2H2O
石墨:2H2O+O2+4e-═4OH-
下列说法中不正确的是( )
| A. | 电子从石墨经外电路流向锌片,电解质溶液为酸性溶液 | |
| B. | 锌片是负极,石墨是正极 | |
| C. | 电池总反应为2Zn+O2═2ZnO | |
| D. | 该原电池工作一段时间后石墨附近溶液中的c(OH-)增大 |
5.下列分子中所有原子都满足最外层8电子结构的是( )
| A. | NH3 | B. | PCl5 | C. | CO2 | D. | CO(NH2)2 |
12.将如图所示实验装置的K闭合,下列判断正确的是( )
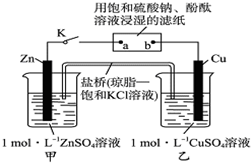

| A. | 电子沿Zn→a→b→Cu路径流动 | B. | Cu电极上发生氧化反应 | ||
| C. | 片刻后可观察到滤纸a点变红色 | D. | 片刻后甲池中c(SO42-)增大 |
2.下列实验装置图(有些图中部分夹持仪器未画出)不能达到其实验目的是( )
| A. | 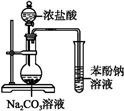 证明酸性:盐酸>碳酸>苯酚 | B. |  实验室制取乙酸乙酯 | ||
| C. |  石油分馏 | D. |  实验室制取硝基苯 |
6.下列物质的转化中,浓HNO3既表现了氧化性,又表现了酸性的是( )
| A. | Cu→Cu(NO3)2 | B. | C→CO2 | C. | CuO→Cu(NO3)2 | D. | Fe2O3→Fe(NO3)3 |
7.可以用分液漏斗分离的一组液体混合物是( )
| A. | 溴和苯 | B. | 苯和溴苯 | C. | 水和硝基苯 | D. | 苯和汽油 |