题目内容
4.写出下列化学方程式:(1)浓硫酸与红热的碳反应C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(2)铜和稀硝酸反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
(3)铝和氢氧化钠溶液反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
分析 (1)红热的炭与浓硫酸加热反应生成二氧化硫和二氧化碳、水;
(2)铜和稀硝酸反应生成硝酸铜、一氧化氮和水;
(3)铝与NaOH溶液反应生成偏铝酸钠和氢气.
解答 解:(1)红热的炭与浓硫酸反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(2)铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(3)铝与NaOH溶液反应生成偏铝酸钠和氢气,化学反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
点评 本题考查了化学方程式的书写注意问题,主要是反应条件,产物判断,侧重于元素化合物知识的综合运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
14.下列关于颜色的描述正确的是( )
①硫单质在纯氧中燃烧--蓝紫色火焰
②淀粉遇到碘化钾溶液--蓝色
③向溴化钠溶液中滴入硝酸银溶液--白色浑浊
④适量的氯气通入KBr溶液--橙黄色
⑤新制氯水久置后--无色
⑥铜在氯气中燃烧产生的烟--棕黄色.
①硫单质在纯氧中燃烧--蓝紫色火焰
②淀粉遇到碘化钾溶液--蓝色
③向溴化钠溶液中滴入硝酸银溶液--白色浑浊
④适量的氯气通入KBr溶液--橙黄色
⑤新制氯水久置后--无色
⑥铜在氯气中燃烧产生的烟--棕黄色.
| A. | ①②③⑤ | B. | ①④⑤⑥ | C. | ②③④⑥ | D. | ①③⑤⑥ |
12.已知X、Y、Z、M四种短周期元素的原子序数依次增大,X与M同主族,X原子的最外层电子数为内层电子数的三倍,Y与X形成的一种化合物常用作潜水艇的供氧剂,Z的氧化物有两性.下列说法正确的是( )
| A. | 最高价氧化物的水化物的碱性:Z>Y | B. | 离子的还原性:M>X | ||
| C. | 电子层数:Y<M | D. | 离子半径:Y<Z |
19.现有一瓶甲和乙的混合液,已知甲和乙的某些性质如表所示:据此,将甲和乙相互分离的最佳方法是( )
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) | 溶解性 |
| 甲 | -68 | 115 | 0.93 | 易溶于水 |
| 乙 | -84 | 77 | 0.90 | 易溶于甲 |
| A. | 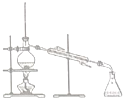 | B. | 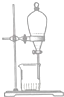 | C. | 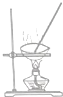 | D. | 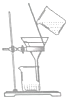 |
9.下列叙述正确的是( )
| A. | 升高反应的温度,会使反应物的活化能迅速降低 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 用电解水的方法制取大量氢气可以缓解能源不足的问题 | |
| D. | 推广使用太阳能、风能等能源,有利于缓解温室效应 |
16.对下列实验的描述正确的是( )
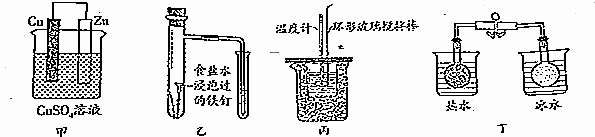

| A. | 图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性 | |
| B. | 图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 | |
| C. | 图丙所示的实验:根据温度计读数的变化用浓硫酸和Na0H反应测定中和热 | |
| D. | 图丁所示的实验:根据两烧瓶中气体颜色的变化判断2N02(g)?N20(g)是吸热反应 |