题目内容
2.在室温下,某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,则此溶液中一定不可能大量存在的离子组是( )| A. | Fe3+、NO3-、Cl-、Na+ | B. | Ca2+、HCO3-、Cl-、K+ | ||
| C. | NH4+、Fe2+、SO42- | D. | Cl-、SO42-、K+、Na+ |
分析 某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,该溶液中存在大量氢离子或氢氧根离子,
A.四种离子之间不发生反应,都不与氢离子反应;
B.碳酸氢根离子与氢离子和氢氧根离子反应;
C.3种离子之间不反应,都不与氢离子反应;
D.四种离子之间不反应,都不与氢离子、氢氧根离子反应.
解答 解:某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,该溶液中存在大量氢离子或氢氧根离子,
A.Fe3+、NO3-、Cl-、Na+之间不反应,都不与氢离子反应,在酸性溶液中能够大量共存,故A错误;
B.HCO3-与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故B正确;
C.NH4+、Fe2+、SO42-之间不发生反应,都不与氢离子反应,在酸性溶液中能够大量共存,故C错误;
D.Cl-、SO42-、K+、Na+之间不发生反应,都不与氢离子和氢氧根离子反应,在溶液中能够大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列化学反应式书写正确的是( )
| A. | 制取氢氧化铁胶体的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3HCl | |
| B. | 亚硫酸在溶液中的电离方程式为H2SO3═2H++SO32- | |
| C. | NaHCO3水解的离子方程式为HCO3-+H2O═CO${\;}_{{3}_{\;}^{\;}}^{2-}$+H3O+ | |
| D. | 泡沫灭火器工作原理离子反应式为 Al3++3 HCO3-═3CO2↑+Al(OH)3↓ |
10.下列反应中氯元素既被氧化又被还原的是( )
| A. | 5Cl2+I2+6H2O═10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | |
| C. | MnO2+4HCl═MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ |
17.能够发生银镜反应且与丙酸互为同分异构体的是( )
| A. | 甲酸乙酯 | B. | 丙醛 | C. | 乙酸甲酯 | D. | 乙酸铵 |
14.下列说法中正确的( )
| A. | 双氧水被称为绿色氧化剂,是因为其还原产物为02,对环境没有污染 | |
| B. | 王水是浓盐酸和硝酸铵按体积比1:3配成的混合液.可以溶解Au、Pt | |
| C. | 氨水能够导电,说明氨气是电解质 | |
| D. | 新制备的氨水中存在三种分子和多种离子 |
11.下列物质既可以用作防腐剂,又可以用作调味剂的是( )
| A. | 酱油 | B. | 食盐 | C. | 味精 | D. | 淀粉 |
12.下列能源符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
| A. | ①②③④ | B. | ⑤⑥⑦⑧ | C. | ④⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
 ,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式:
,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式: +2NaOH$\stackrel{△}{→}$HCOONa+
+2NaOH$\stackrel{△}{→}$HCOONa+ +H2O.
+H2O.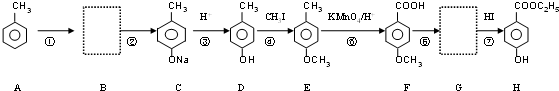
 .反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)
.反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)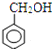 或
或 .
. .
.