题目内容
17.能够发生银镜反应且与丙酸互为同分异构体的是( )| A. | 甲酸乙酯 | B. | 丙醛 | C. | 乙酸甲酯 | D. | 乙酸铵 |
分析 能够发生银镜反应的有机物分子中一定含有醛基,与丙酸互为同分异构体,说明该有机物与丙酸具有相同的分子式、不同的结构,据此进行判断.
解答 解:A.甲酸乙酯与丙酸的分子式相同,结构不同,二者互为同分异构体,并且甲酸乙酯中含有醛基,能够发生银镜反应,故A正确;
B.丙醛与丙酸的分子式不同,二者不属于同分异构体,故B错误;
C.乙酸甲酯与丙酸的分子式相同,结构不同,二者互为同分异构体,分子中不含有醛基,不能发生银镜反应,故C错误;
D.乙酸铵与丙酸的分子式不同,二者不属于同分异构体,分子中不含有醛基,不能发生银镜反应,故D错误;
故选A.
点评 本题考查了有机物结构与性质、同分异构体的判断,题目难度不大,注意掌握常见有机物结构与性质,明确甲酸与醇生成的酯中含有醛基,能够发生银镜反应.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
7.下列物质中,不属于合金的是( )
| A. | 硬铝 | B. | 黄铜 | C. | 纯铁 | D. | 生铁 |
5.下列说法正确的有几项( )
①pH≤5.6的降水称酸雨
②NO2是HNO3的酸酐
③硅酸凝胶即为硅胶
④干燥的氯气也有漂白性
⑤常温下可以用铁桶盛装浓硝酸
⑥Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性.
①pH≤5.6的降水称酸雨
②NO2是HNO3的酸酐
③硅酸凝胶即为硅胶
④干燥的氯气也有漂白性
⑤常温下可以用铁桶盛装浓硝酸
⑥Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性.
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
12.从降低成本和绿色化学的角度考虑,制取硝酸铜最好的方法是( )
| A. | 为了防止硝酸分解生成有毒气体和减少硝酸的挥发,在常温下,用铜和浓硝酸反应 | |
| B. | 为了防止污染物的生成,让铜和稀硫酸反应 | |
| C. | 铜先在空气中加热生成氧化铜,然后再和硝酸反应 | |
| D. | 氯化铜和硝酸银恰好完全反应生成硝酸铜和氯化银,然后过滤除去氯化银沉淀 |
2.在室温下,某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,则此溶液中一定不可能大量存在的离子组是( )
| A. | Fe3+、NO3-、Cl-、Na+ | B. | Ca2+、HCO3-、Cl-、K+ | ||
| C. | NH4+、Fe2+、SO42- | D. | Cl-、SO42-、K+、Na+ |
9.下列说法正确的是( )
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-(Ea-Eb) kJ/mol | |
| B. | 某温度下,氯化钠在水中的溶解度是20 g,则该温度下的饱和氯化钠溶液溶质的质量分数为20% | |
| C. | 将0.2 mol/L 的CH3COOH 溶液与0.1 mol/L 的NaOH 溶液等体积混合后,溶液中有关粒子的浓度满足下列关系:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| D. | 将浓度为0.1 mol/L HF 溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
6.下列物质中,主要成分不是SiO2的是( )
| A. | 金刚砂 | B. | 玛瑙 | C. | 水晶 | D. | 石英 |
7.下列有机化学反应方程式书写不正确的是( )
| A. | CH2=CH2+Cl2→CH2ClCH2Cl | B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | ||
| C. | 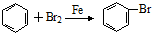 | D. | 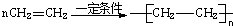 |