题目内容
【题目】将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A.1∶2∶3B.6∶3∶2C.3∶1∶1D.1∶1∶1
【答案】C
【解析】
将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,根据方程式可知三种金属都是足量,应按盐酸的量计算产生氢气的量,因为镁、铝产生氢气物质的量相等,所以由Mg+2HCl=MgCl2+H2↑可知:产生氢气的物质的量为:(0.1L![]() 1mol/L)
1mol/L)![]() =0.05mol,因为金属钠活泼,能与水反应生成氢气,则生成氢气最多的是钠,钠与盐酸和水能完全反应,所以产生氢气应按钠的物质的量计算:2Na
=0.05mol,因为金属钠活泼,能与水反应生成氢气,则生成氢气最多的是钠,钠与盐酸和水能完全反应,所以产生氢气应按钠的物质的量计算:2Na![]() H2↑,0.3mol钠产生0.15mol氢气;所以同温同压下产生的气体体积比是3∶1∶1,故C符合题意;
H2↑,0.3mol钠产生0.15mol氢气;所以同温同压下产生的气体体积比是3∶1∶1,故C符合题意;
答案:C。

练习册系列答案
相关题目
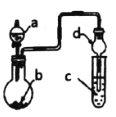
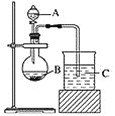
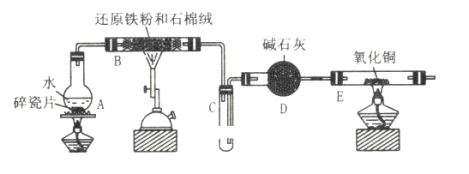
【题目】用如图装置进行实验,将液体a逐滴加到固体b中,下列叙述正确的是
选项 | a | b | c | 现象 | 装置图 |
A | 浓H2SO4 | Cu | 澄清石灰水 | c中溶液变浑浊 |
|
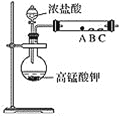
B | 浓盐酸 | KMnO4晶体 | 紫色石蕊溶液 | c中溶液最终呈红色 | |
C | 稀HNO3 | Fe | NaOH溶液 | d中红棕色气体变浅 | |
D | 浓氨水 | 生石灰 | Al2(SO4)3溶液 | c中产生沉淀后溶解 |
A.AB.BC.CD.D
【题目】在容积一定的密闭容器中发生可逆反应A(g)+B(g)![]() C(g) △H>0,平衡移动关系如下图所示下列说法正确的是
C(g) △H>0,平衡移动关系如下图所示下列说法正确的是
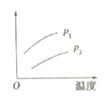
选项 | 压强 | 纵坐标 |
A | p1>p2 | B的转化率 |
B | p1<p2 | C的物质的量浓度 |
C | p1<p2 | 混合气体的平均摩尔质量 |
D | p1>p2 | A的质量分数 |
A. AB. BC. CD. D