��Ŀ����
����Ŀ��ijУ��ѧС��ѧ��������ͼ����װ�ý��� ������ˮ��Ӧ����ʵ�飬�����ò����һ����ȡFeCl3��6H2O���塣(ͼ�мгּ�β������װ�þ�����ȥ)
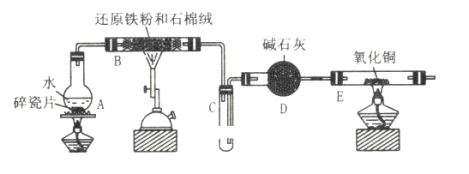
��1��װ��B�з�����Ӧ�Ļ�ѧ����ʽ��__��
��2��װ��E�е������ǣ�__��
��3��ֹͣ��Ӧ����B����ȴ��ȡ���еĹ��壬�������ϡ�����ַ�Ӧ�����ˡ�����������Һ��Fe3+�IJ���������__��
��4����С��ѧ������������Һ��ȡFeCl3��6H2O���壬����������£�
![]()
����I��ͨ��Cl2��������__��
���𰸡�3Fe+4H2O(g)![]() Fe3O4+4H2 ��ɫ�����Ϊ��ɫ���ܱ���ˮ�� ȡ������Һ�����뼸��KSCN��Һ���۲���Һ�Ƿ���ɫ ����Һ�к��е�Fe2+������Fe3+
Fe3O4+4H2 ��ɫ�����Ϊ��ɫ���ܱ���ˮ�� ȡ������Һ�����뼸��KSCN��Һ���۲���Һ�Ƿ���ɫ ����Һ�к��е�Fe2+������Fe3+
��������
A��Բ����ƿ�ڼ��������¿��ṩˮ������B�ڼ��������£�����ˮ������Ӧ���������������������������������C���������ſշ����ռ���������DΪ����װ�ã��ڼ�������������������ͭ��Ӧ����ͭ��ˮ������KSCN���������ӣ��Դ˽�����
(1)����ˮ���������·�Ӧ�����������������������ݴ�д����Ӧ�Ļ�ѧ����ʽ��
(2)װ��E�к�ɫ����������������ԭ�ɺ�ɫ������ͬʱ��ˮ�����ɣ�
(3)B�ڼ��������£�����ˮ������Ӧ����������������������ֹͣ��Ӧ����B����ȴ��ȡ���еĹ��壬����ijɷֿ���Ϊ�����������������ڹ����м������ϡ���������������������������֮��ķ�Ӧ������KSCN���������ӣ�
(4)��Һ����![]() ��ͨ��������
��ͨ�������� ![]() ������
������![]() ���ٽ�
���ٽ�![]() ϡ��Һ���м���Ũ������ȴ�ᾧ�����˼���FeCl3��6H2O���壻
ϡ��Һ���м���Ũ������ȴ�ᾧ�����˼���FeCl3��6H2O���壻
(1)װ��B��������ˮ�����ڸ����·�����Ӧ������������������������Ӧ�Ļ�ѧ����ʽΪ:![]() �ʴ�Ϊ
�ʴ�Ϊ ![]() ��
��
(2)װ��B����ˮ������Ӧ���ɵ�����������ʯ�Ҹ�������װ��E������ͭ���������ȷ�����Ӧ������ͭ��ˮ�����Է�Ӧ������Ϊ����ɫ�ķ�ĩ����Ϻ�ɫ���ܱڲ���ˮ�飬�ʴ�Ϊ����ɫ�ķ�δ����Ϻ�ɫ���� �ڲ���ˮ�飻
(3) ȡ������Һ�����뼸��KSCN��Һ���۲���Һ�Ƿ���ɫ��
(4)��Ϊ��������ǿ�����ԣ������ܽ�����������Ϊ���������ʴ�Ϊ����Һ�к��е�Fe2+������Fe3+

 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�����Ŀ��CH4-CO2�������������Եõ��ϳ�����CO��H2����������������ļ��ž�����Ҫ���塣�ش��������⣺
��1��CH4-CO2��������ӦΪ��CH4(g)+CO2(g)=2CO(g)+2H2(g)��
��֪��C(s)+2H2(g)=CH4(g) ��H=-75 kJ��mol1
C(s)+O2(g)=CO2(g) ��H=-394 kJ��mol1
C(s)+1/2O2(g)=CO(g) ��H=-111 kJ��mol1
�ô�������Ӧ����H==______ kJ��mol1�����������CH4ƽ��ת���ʵ�������____�����ţ���
A�����µ�ѹ B�����¸�ѹ C�����¸�ѹ D�����µ�ѹ
ij�¶��£������Ϊ2 L�������м���2 mol CH4��1 mol CO2�Լ���������������Ӧ���ﵽƽ��ʱCO2��ת������50%����ƽ�ⳣ��Ϊ_______mol2��L2��
��2����Ӧ�д������Ի����̼��Ӧ�����ͣ�ͬʱ���ڵ���̼��Ӧ��ʹ��̼�����١�
����������±���
��̼��Ӧ CH4(g)=C(s)+2H2(g) | ��̼��Ӧ CO2(g)+C(s)=2CO(g) | ||
��H/(kJ��mol1) | 75 | 172 | |
���/ (kJ��mol1) | ����X | 33 | 91 |
����Y | 43 | 72 | |
�����ϱ��жϣ�����X____Y��������������������������������_________________���ڷ�Ӧ��������ɡ�ѹǿ����Ӧʱ����ͬ������£�ij��������Ļ�̼�����¶ȵı仯��ϵ��ͼ��ʾ�������¶�ʱ�����й��ڻ�̼��Ӧ����̼��Ӧ��ƽ�ⳣ����K�������ʣ�v����������ȷ����________���ţ���

A��K����K�������� B��v������v������
C��K����С��K������ D��v�����ӵı�����v�����ӵı�����
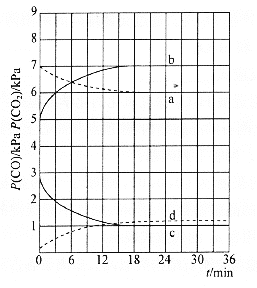
����һ���¶��£����ij�����ϳ���̼���������ʷ���Ϊv=k��p(CH4)��[p(CO2)]-0.5��kΪ���ʳ���������p(CH4)һ��ʱ����ͬp(CO2)�»�̼����ʱ��ı仯������ͼ��ʾ����pa(CO2)��pb(CO2)��pc(CO2)�Ӵ�С��˳��Ϊ________________��