题目内容
 某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)
(2)判断滴定终点的现象是:
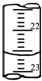
(3)如图是某次滴定时的滴定管中的液面,其读数为
(4)根据下列数据:请计算待测盐酸溶液的浓度:
| 滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
考点:中和滴定
专题:
分析:(1)碱式滴定管洗涤后必须用标准液氢氧化钠溶液润洗;根据不润洗会使标准液的浓度偏小判断对测定结果影响;
(2)根据滴定终点前溶液为无色,滴定结束时氢氧化钠过量,溶液显示红色判断滴定终点;
(3)根据滴定管的构造及图示读出滴定管的读数;
(4)根据表中消耗的标准液的数据先判断数据的有效性,然后计算出消耗标准液的平均体积,最后计算出待测液盐酸的浓度.
(2)根据滴定终点前溶液为无色,滴定结束时氢氧化钠过量,溶液显示红色判断滴定终点;
(3)根据滴定管的构造及图示读出滴定管的读数;
(4)根据表中消耗的标准液的数据先判断数据的有效性,然后计算出消耗标准液的平均体积,最后计算出待测液盐酸的浓度.
解答:
解:(1)“①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液”,该操作错误,碱式滴定管应该润洗后再盛装标准液,若没有润洗,导致标准液的浓度减小,滴定时消耗的标准液的体积偏大,测定结果偏大,
故答案为:①;偏大;
(2)滴定结束前,锥形瓶中滴入酚酞,溶液为无色,滴定结束后,滴入氢氧化钠溶液后,溶液显示粉红色,所以达到终点的现象为:锥形瓶中溶液无色变为粉红,半分钟内不变色,
故答案为:无色变为粉红,半分钟内不变色;
(3)根据图示滴定管结构可知,每个小刻度为0.01mL,液面凹液面在22mL刻度以下6个小刻度,读数为22.60mL,
故答案为:22.60;
(4)根据表中数据,第一次滴定消耗的标准液体积为:(20.40-0.40)mL=20.00mL,
第二次滴定消耗的标准液体积为:(24.10-2.00)mL=22.10mL,
第三次滴定消耗的标准液体积为:(24.00-4.00)mL=20.00mL,
可见第二次滴定数据误差偏大,应该舍弃,其它两次滴定消耗的标准液平均体积为:20.00mL,
氢氧化钠和盐酸都是一元酸,反应的体积都是20.00mL,所以氢氧化钠溶液和盐酸的浓度一定相等,即盐酸的浓度为:0.2000mol?L-1,
故答案为:0.2000.
故答案为:①;偏大;
(2)滴定结束前,锥形瓶中滴入酚酞,溶液为无色,滴定结束后,滴入氢氧化钠溶液后,溶液显示粉红色,所以达到终点的现象为:锥形瓶中溶液无色变为粉红,半分钟内不变色,
故答案为:无色变为粉红,半分钟内不变色;
(3)根据图示滴定管结构可知,每个小刻度为0.01mL,液面凹液面在22mL刻度以下6个小刻度,读数为22.60mL,
故答案为:22.60;
(4)根据表中数据,第一次滴定消耗的标准液体积为:(20.40-0.40)mL=20.00mL,
第二次滴定消耗的标准液体积为:(24.10-2.00)mL=22.10mL,
第三次滴定消耗的标准液体积为:(24.00-4.00)mL=20.00mL,
可见第二次滴定数据误差偏大,应该舍弃,其它两次滴定消耗的标准液平均体积为:20.00mL,
氢氧化钠和盐酸都是一元酸,反应的体积都是20.00mL,所以氢氧化钠溶液和盐酸的浓度一定相等,即盐酸的浓度为:0.2000mol?L-1,
故答案为:0.2000.
点评:本题考查了酸碱中和滴定、pH的简单计算、离子方程式的书写,题目难度不大,注重了中和滴定的基础知识考查,要求学生掌握中和滴定的方法.

练习册系列答案
相关题目
用NA代表阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下,2.24LCHCl3的分子数0.1NA |
| B、1molNH3中含有3NA对电子 |
| C、9.2g NO2和N2O4的混合气中含有的氮原子数为大于0.2NA |
| D、某氯化铁溶液中Fe3+的数目为NA,则Cl-的数目大于3NA |
跟mg CO2中所含的氧原子数相等的KMnO4的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列的说法中正确的是( )
| A、钠的还原性很强,在空气中易变质,久置后变为过氧化钠 |
| B、氢氧化钠溶液可长时间保存在带磨口玻璃塞的试剂瓶中 |
| C、新制的氯水通常保存在棕色玻璃试剂瓶中,并现用现配 |
| D、漂粉精的有效成分为氯化钙 |
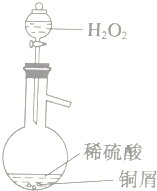
 I.某中和滴定实验过程如下:
I.某中和滴定实验过程如下: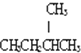 ;D:
;D: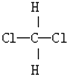 和
和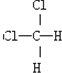

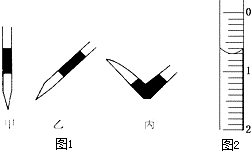 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.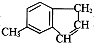 )是一种医药合成中间体,某同学设计它的合成路线如下:
)是一种医药合成中间体,某同学设计它的合成路线如下: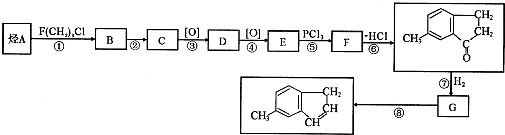
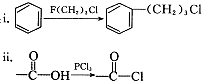
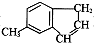 )的说法正确的是
)的说法正确的是