题目内容
10.下列物质既能通过化合反应,又能通过复分解反应生成的是( )①Fe(OH)3 ②Fe(NO3)2 ③NaHCO3 ④Al2S3 ⑤NH4Cl ⑥NaOH.
| A. | ④除外都可以 | B. | 除②④外都可以 | C. | 只有①⑤⑥可以 | D. | 全部都可以 |
分析 由两种或两种以上的物质生成一种物质的反应为化合反应;两种化合物相互交换成分生成另外两种化合物的反应为复分解反应,据此分析.
解答 解:①Fe(OH)3 可以通过化合反应4Fe(OH)2+O2+2H2O=4Fe(OH)3生成,还可以通过复分解反应FeCl3+3NaOH=Fe(OH)3+3NaCl生成,故①正确;
②Fe(NO3)2 可以通过化合反应2Fe(NO3)3+Fe=3Fe(NO3)2 生成,还可以通过复分解反应FeCl2+2AgNO3=2AgCl↓+Fe(NO3)2生成,故②正确;
③NaHCO3 可以通过化合反应Na2CO3+CO2+H2O=2NaHCO3生成,还可以通过复分解反应Ca(HCO3)2+Na2CO3=2NaHCO3+CaCO3↓生成,故③正确;
④由于Al2S3 在溶液中能发生双水解,故不能通过复分解反应制取,只能通过铝和硫的化合制取:2Al+3S$\frac{\underline{\;加热\;}}{\;}$Al2S3,故④错误;
⑤NH4Cl可以通过化合反应NH3+HCl=NH4Cl制取,也可以通过复分解反应HCl+NH3•H2O=NH4Cl+H2O制取,故⑤正确;
⑥NaOH可以通过化合反应Na2O+H2O=2NaOH来制取,也可以通过复分解反应Ca(OH)2+Na2CO3=CaCO3↓+2NaOH制取,故⑥正确.
故选A.
点评 本题考查了常见物质的性质,难度不大,熟练掌握物质的性质是解题的关键,应注意的是由于Al2S3 在溶液中能发生双水解,故其制取不能在溶液中进行.

练习册系列答案
相关题目
18.在100mL下列溶液中,分别加入0.05molNaOH固体,溶液的导电能力变化不大的是( )
| A. | 蒸馏水 | B. | 0.5 mol/L的醋酸溶液 | ||
| C. | 0.5 mol/L的盐酸 | D. | 0.5 mol/L的氨水 |
5. 利用如图1装置测定中和热的实验步骤如下:
利用如图1装置测定中和热的实验步骤如下:
①用量筒量取50mL0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度.回答下列问题:
(1)仪器A的名称为环形玻璃搅拌棒.
(2)写成稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol)$\frac{1}{2}$H2SO4(l)+NaOH(l)=$\frac{1}{2}$Na2SO4(l)+H2O(l)△H=-57.3KJ/mol.
(3)倒入NaOH溶液的正确操作是C(填序号).
A.沿玻璃棒缓慢倒入B.分三次少量倒入C.一次迅速倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是E(从下列选出)D.
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(5)实验数据如下表:
①请填写下表中的空白:
②近似认为0.55mol/LNaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8kJ/mol(取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(6)将V1mL1.0mol/LHCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL).则NaOH溶液的物质的量浓度为1.5 mol•L-1.
 利用如图1装置测定中和热的实验步骤如下:
利用如图1装置测定中和热的实验步骤如下:①用量筒量取50mL0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度.回答下列问题:
(1)仪器A的名称为环形玻璃搅拌棒.
(2)写成稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol)$\frac{1}{2}$H2SO4(l)+NaOH(l)=$\frac{1}{2}$Na2SO4(l)+H2O(l)△H=-57.3KJ/mol.
(3)倒入NaOH溶液的正确操作是C(填序号).
A.沿玻璃棒缓慢倒入B.分三次少量倒入C.一次迅速倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是E(从下列选出)D.
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(5)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2℃ | 温度差平均值(t2-t1)℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(6)将V1mL1.0mol/LHCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL).则NaOH溶液的物质的量浓度为1.5 mol•L-1.
2.已知下述三个实验均能发生化学反应:
下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴氯水 | 将铜丝放入氯化铁溶液中 |
| A. | 实验①中铁钉只做还原剂 | |
| B. | 实验②中Fe2+既显氧化性又显还原性 | |
| C. | 实验③中发生的是置换反应 | |
| D. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
19.下列关于醋酸钠溶液的说法中正确的是( )
| A. | 溶液呈酸性 | B. | c(H+)=c(CH3COO-)+c(OH-) | ||
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | D. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
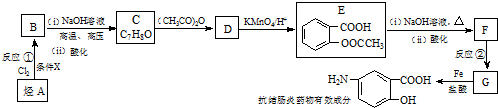
 $\stackrel{(CH_{3}CO)_{2}O}{→}$
$\stackrel{(CH_{3}CO)_{2}O}{→}$ (b)
(b)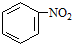 $→_{盐酸}^{Fe}$
$→_{盐酸}^{Fe}$
 ;
;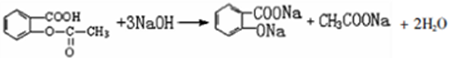 ;
; ;
; )易被氧化,苯环上连有烷基时再引入一个取代基,常取代
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代 ) 合成路线中两种中间产物的结构简式(部分反应条
) 合成路线中两种中间产物的结构简式(部分反应条 .
.
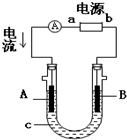 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题: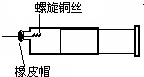 某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.
某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.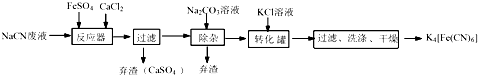
 .
.