题目内容
已知:20℃时NaHCO3溶解度为9.6g,将CO2通入Na2CO3饱和溶液中,产生白色固体,该固体是 ,请解释产生原因: .
考点:钠的重要化合物
专题:元素及其化合物
分析:CO2通入Na2CO3饱和溶液中,发生Na2CO3+CO2+H2O=2NaHCO3,因NaHCO3溶解度较小,沉淀为NaHCO3,以此解答该题.
解答:
解:Na2CO3比NaHCO3易溶于水,在饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,发生Na2CO3+CO2+H2O=2NaHCO3,
故答案为:NaHCO3;反应生成溶解度更小的NaHCO3.
故答案为:NaHCO3;反应生成溶解度更小的NaHCO3.
点评:本题考查NaHCO3性质,侧重于学生的分析能力的考查,为高频考点,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
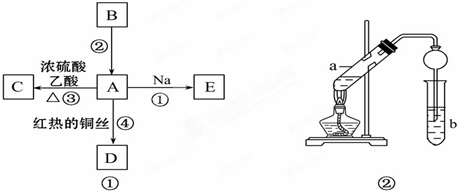
下列变化:①导电、②爆炸、③缓慢氧化、④变色、⑤无水硫酸铜吸水、⑥工业制氧气、⑦白磷变成红磷、⑧久置浓HNO3变黄,一定属于化学变化的是( )
| A、①④ | B、⑥⑧ |
| C、②⑥⑦ | D、③⑤⑦⑧ |
短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的颜色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z元素的核电荷数是W的2倍,Y是地壳中含量最多的金属元素.下列说法不正确的是( )
| A、工业上常用电解的方法制备X、Y的单质 |
| B、元素Q和Z能形成QZ2型的共价化合物 |
| C、原子半径的大小顺序:r(X)>r(Y)>r(W)>r(Q) |
| D、元素X、Y的最高价氧化物对应的水化物之间能发生反应 |
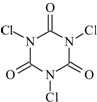 三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.
三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.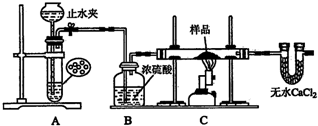 某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:
某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下: