题目内容
14.自制胶水的方法之一是将废旧高分子材料切碎后用汽油浸泡-段时间,待其溶解后,即可作胶水使用.下列材料可作该项用途的是( )| A. | 硫化橡胶 | B. | 酚醛树脂 | C. | 聚乙烯塑料 | D. | 硝酸纤维 |
分析 线型高分子材料一般易溶于有机溶剂,其弹性较好,据此分析.
解答 解:线型高分子材料一般易溶于有机溶剂,其弹性较好,而体型高分子材料弹性差且难溶于有机溶剂,而聚乙烯塑料为线型高分子化合物,故可溶于汽油制成胶水,
故选C.
点评 本题考查了高分子化合物的结构和性质特点,难度不大,注意线型高分子材料和体型高分子材料的区别.

练习册系列答案
相关题目
4.我国南朝(梁)陶弘景著《本草经集注》中记叙药物730种,其中“消石”条目下写道:“…如握雪不冰.强烧之,紫青烟起,仍成灰…”.这里的“消石”是指( )
| A. | 氯化钠 | B. | 硝酸按 | C. | 高锰酸钾 | D. | 硝酸钾 |
2.下列有关物质的性质和应用都正确的是( )
| A. | BaSO4的水溶液不导电,故BaSO4是弱电解质 | |
| B. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也不存在同分异构体 | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | AgCl在同温、同浓度的CaCl2和NaCl溶液中的溶解度不同 |
9.W、X、Y、Z是1-20号元素中的四种元素,原子序数依次增大;W的主要化合价为-2价,原子半径为0.074nm,X所在的主族序数与所在的周期序数之差为3;Y原子最外层电子数为奇数;Z最高价氧化物对应的水化物电离出的阴、阳离子数目相等,下列说法正确的是( )
| A. | W可能是氧元素,也可能是硫元素 | |
| B. | X元素氧化物对应的水化物一定是一种强酸 | |
| C. | Y元素原子次外层电子数与最外层电子敦之差为1 | |
| D. | Z可能是氯元素,也可能是钾元素 |
19.下列物质在室温下的溶解度最小的是( )
| A. | 硫酸铵 | B. | 绿矾 | C. | 摩尔盐 | D. | 硫酸 |
6.关于蛋白质的说法下列正确的是( )
| A. | 天然蛋白质中仅含C、H、0、N四种元素 | |
| B. | 加入(NH4)2S04饱和溶液会使蛋白质变性 | |
| C. | 重金属盐能使蛋白质凝结,所以误食重金属盐会中毒 | |
| D. | 鸡蛋清加入食盐,会使蛋白质变性 |
6. 某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
①称取W g样品,准确配成500mL溶液.
②准确配制0.1000mol/L的标准盐酸.
③用滴定管取所配制碱液25.00mL于锥形瓶,并向瓶中滴几滴甲基橙试液.
④向锥形瓶中逐滴滴入标准盐酸,直到终点.
⑤记录数据,计算.请回答:
(1)在①操作中要使用的定量的玻璃仪器是500ml容量瓶.
(2)操作④装标准盐酸的滴定管是酸式滴定管.
(3)滴定过程中左手控制酸式滴定管的活塞,右手向一个方向摇动锥形瓶.眼睛应始终注视锥形瓶内溶液的颜色变化,判断滴定到达终点的现象是滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
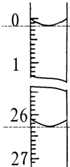
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10ml.
(5)某学生根据3次实验分别记录有关数据如表:
②依据上表数据列式计算该NaOH溶液的物质的量浓度(计算结果取4位有效数).
③根据上面结果计算NaOH的纯度$\frac{2.096}{W}$×100%.
(6)下列操作中,可能使测定结果偏低的是ACF.
A.称取样品时,样品和砝码位置放反了
B.配制标准盐酸过程中,读取量筒读数时,俯视刻度线
C.碱式滴定管清洗后,未用待测液润洗
D.酸式滴定管清洗后,未用待测液润洗
E.锥形瓶装液前未干燥,有水珠附着在瓶壁
F.读取酸式滴定管读数时,第一次读数仰视,第二次读数俯视.
 某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:①称取W g样品,准确配成500mL溶液.
②准确配制0.1000mol/L的标准盐酸.
③用滴定管取所配制碱液25.00mL于锥形瓶,并向瓶中滴几滴甲基橙试液.
④向锥形瓶中逐滴滴入标准盐酸,直到终点.
⑤记录数据,计算.请回答:
(1)在①操作中要使用的定量的玻璃仪器是500ml容量瓶.
(2)操作④装标准盐酸的滴定管是酸式滴定管.
(3)滴定过程中左手控制酸式滴定管的活塞,右手向一个方向摇动锥形瓶.眼睛应始终注视锥形瓶内溶液的颜色变化,判断滴定到达终点的现象是滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10ml.
(5)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V=26.20 |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
③根据上面结果计算NaOH的纯度$\frac{2.096}{W}$×100%.
(6)下列操作中,可能使测定结果偏低的是ACF.
A.称取样品时,样品和砝码位置放反了
B.配制标准盐酸过程中,读取量筒读数时,俯视刻度线
C.碱式滴定管清洗后,未用待测液润洗
D.酸式滴定管清洗后,未用待测液润洗
E.锥形瓶装液前未干燥,有水珠附着在瓶壁
F.读取酸式滴定管读数时,第一次读数仰视,第二次读数俯视.
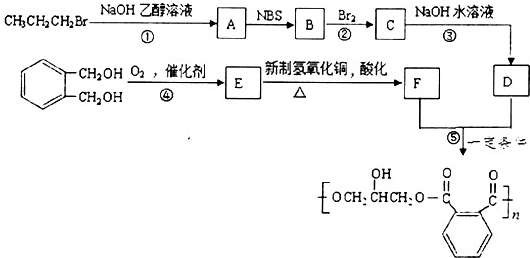
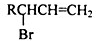
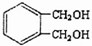 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式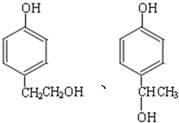 (其中之一);
(其中之一);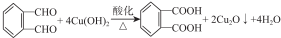 ;
;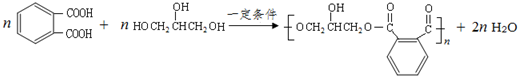 .
.