题目内容
2.下列有关物质的性质和应用都正确的是( )| A. | BaSO4的水溶液不导电,故BaSO4是弱电解质 | |
| B. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也不存在同分异构体 | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | AgCl在同温、同浓度的CaCl2和NaCl溶液中的溶解度不同 |
分析 A.硫酸钡是难溶的盐,熔融状态完全电离;
B.分子式相同结构不同的有机物互为同分异构体;
C.反应的△S<0,能自发,说明△H<0;
D.CaCl2和NaCl溶液中都含有氯离子,所以都能抑制氯化银溶解,且氯离子浓度越大,其抑制程度越大.
解答 解;A.硫酸钡是难溶的盐,熔融状态完全电离,属于强电解质,故A错误;
B.甲醚与乙醇为同分异构体,故B错误;
C.2Mg(s)+CO2(g)═C(s)+2MgO(s),该反应的△S<0,能自发,说明△H<0,故C错误;
D.CaCl2和NaCl溶液中都含有氯离子,都抑制了氯化银的溶解,且氯离子浓度越大,其抑制程度越大,所以AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度不同,故D正确;
故选:D.
点评 本题为综合题,涉及电解质强弱的判断、同分异构体判断、反应自发进行方向的判断、沉淀溶解平衡移动影响因素,熟悉相关知识即可解答,题目难度不大,注意电解质强弱与电离程度有关,与溶解性、导电性无关.

练习册系列答案
相关题目
12.下列关于各图象的解释或得出结论正确的是( )
| A. | 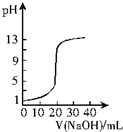 图表示0.10 mol•L-1 NaOH溶液滴定20.00 mL 0.10 mol•L-1醋酸溶液的滴定曲线 | |
| B. | 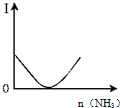 图表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化 | |
| C. | 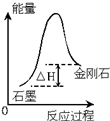 根据图所示可知:金刚石生成石墨为放热反应 | |
| D. | 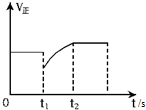 图表示反应2SO2+O2?2SO3,t1时刻只小了的SO3的浓度 |
10.下列叙述正确的是( )
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同质子数相同的同种核素 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
17.有a、b、c、d四种元素,均为原子序数依次增大的前20号元素.a存在a+和a-两种 离子,b和c为同一主族元素,c的次外层有8个电子,c2-和d2+的电子层结构相同.下列叙述正确的是( )
| A. | b、c与a形成化合物的稳定性一定为c>b | |
| B. | a和d形成的化合物与水反应产生气体可以作燃料 | |
| C. | c、a和b可形成的化合物为离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可以为酸性、也可以为碱性 |
14.自制胶水的方法之一是将废旧高分子材料切碎后用汽油浸泡-段时间,待其溶解后,即可作胶水使用.下列材料可作该项用途的是( )
| A. | 硫化橡胶 | B. | 酚醛树脂 | C. | 聚乙烯塑料 | D. | 硝酸纤维 |
11.在室温下,0.1mol•L-1100ml 的醋酸溶液中,欲使其溶液的c(H+)增大,但又要使醋酸电离程度减少,应采取( )
| A. | 加入少量CH3COONa固体 | B. | 通入少量氯化氢气体 | ||
| C. | 提高温度 | D. | 加入少量纯醋酸 |
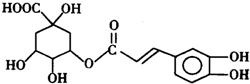 .
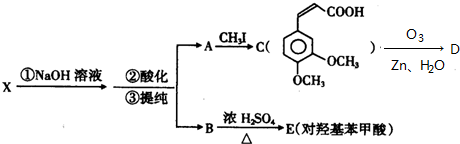
.
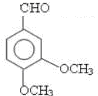 ;
;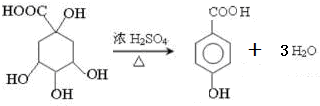 ;
;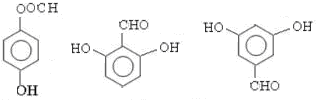 任意一种;(任写一种)
任意一种;(任写一种)