题目内容
8. 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍.写出在潮湿空气中钢铁锈蚀时发生还原反应的电极电应式:O2+4e-+2H2O=4OH-,将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并末检测出Fe3+,用离子方程式说明原因:2Fe3++Fe=3Fe2+.
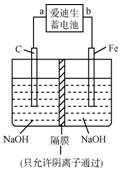
(2)爱迪生蓄电池的反应式为Fe+NiO2+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂.用如图装置可以制取少量高铁酸钠.
①此装置中爱迪生蓄电池的负极是a(填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是氧化反应.
②写出在用电解法制取高铁酸钠时,阳极的电极反应式Fe-6e-+8OH-=FeO42-+4H2O.
③你认为高铁酸钠作为一种新型净水剂的理由可能是BC.
A.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
B.高铁酸钠具有强氧化性,能消毒杀菌
C.高铁酸钠在消毒杀菌时被还原生成Fe3+,水解产生氢氧化铁胶体能吸附悬浮杂质.
分析 (1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上得电子发生还原反应;铁和铁离子能发生氧化还原反应生成亚铁离子;
(2)①放电时,铁棒作负极,碳棒作正极,据此判断a的电极;失电子的物质发生氧化反应;
②铁失电子和氢氧根离子生成高铁酸根离子和水;
③高铁酸根离子有强氧化性,被还原生成的三价铁离子能发生生成胶体,胶体具有吸附性.
解答 解:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上氧气得电子和水反应生成氢氧根离子O2+4e-+2H2O=4OH-;铁和铁离子能发生氧化还原反应生成亚铁离子,离子方程式为:2Fe3++Fe=3Fe2+,导致溶液中不存在铁离子;
故答案为:O2+4e-+2H2O=4OH-;2Fe3++Fe=3Fe2+;
(2)①放电时,铁作负极,碳棒作正极,所以放电时a是负极,b是正极;充电时,氢氧化镍失电子生成氧化镍,发生氧化反应;
故答案为:a;氧化反应;
②阳极上铁失电子和氢氧根离子反应生成高铁酸根离子和水,离子方程式为:Fe-6e-+8OH-=FeO42-+4H2O;
故答案为:Fe-6e-+8OH-=FeO42-+4H2O;
③高铁酸钠具有强氧化性,所以能杀菌消毒;高铁酸钠能被还原生成铁离子,铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,能吸附悬浮杂质,所以能净水;
故选BC.
点评 本题以安迪生电池为载体考查了原电池原电池和电解池原理,难度不大,明确高铁酸钠能作为一种新型净水剂的原理.

练习册系列答案
相关题目
18.下列关于元素及其化合物的说法不正确的是( )
| A. | Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应 | |
| B. | Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解 | |
| D. | 金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱 |
19.19世纪末,开始揭开原子内部的秘密,最早发现电子的科学家是( )
| A. | 英国的道尔顿 | B. | 英国的卢瑟福 | C. | 丹麦的玻尔 | D. | 英国的汤姆生 |
16.柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( )
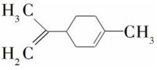

| A. | 柠檬烯的一氯代物有7种 | |
| B. | 柠檬烯和丁基苯互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | 在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应 |
3.元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中错误的是( )
| A. | 次氯酸的电子式: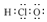 | B. | S2-的结构示意图: | ||
| C. | O-18的原子符号:${\;}_{\;}^{15}$O | D. | CO2分子的结构式:O=C=O |
13.X和Y均为短周期元素,X原子的最外层电子数是次外层电子数的2.5倍,Y原子是原子半径最小的原子,则X和Y形成的化合物的分子式可表示为( )
| A. | XY | B. | XY2 | C. | XY3 | D. | XY4 |
20.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气体 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 元素B的单质可被热的浓硫酸或浓硝酸氧化 | |
| D. | 化合物AE与CE含有相同类型的化学键 |