题目内容
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温常压下,9gH2O含有分子数为0.5NA |
| B、标准状况下,以任意比例混合的甲烷和丙烷(C3H8)的气体混合物11.2L,则所含有的分子数为NA |
| C、常温常压下,活泼金属从盐酸中置换出1molH2时发生转移的电子数为2NA |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.9g水的物质的量为:
=0.5mol;
B.标准状况下,11.2L甲烷和丙烷的混合气体的物质的量为0.5mol;
C.活泼金属与足量盐酸反应,每生成1mol氢气,需要转移2mol电子;
D.缺少氯化镁溶液的体积,无法计算溶液中氯离子的数目.
| 9g |
| 18g/mol |
B.标准状况下,11.2L甲烷和丙烷的混合气体的物质的量为0.5mol;
C.活泼金属与足量盐酸反应,每生成1mol氢气,需要转移2mol电子;
D.缺少氯化镁溶液的体积,无法计算溶液中氯离子的数目.
解答:
解:A.9g水的物质的量为0.5mol,含有分子数为0.5NA,故A正确;
B.标准状况下,以任意比例混合的甲烷和丙烷(C3H8)的气体混合物11.2L,其物质的量为0.5mol,所含有的分子数为0.5NA,故B错误;
C.常温常压下,活泼金属从盐酸中置换出1molH2时转移了2mol电子,发生转移的电子数为2NA,故C正确;
D.没有告诉0.5mol/L MgCl2溶液的体积,无法计算溶液中氯离子的数目,故D错误;
故选AC.
B.标准状况下,以任意比例混合的甲烷和丙烷(C3H8)的气体混合物11.2L,其物质的量为0.5mol,所含有的分子数为0.5NA,故B错误;
C.常温常压下,活泼金属从盐酸中置换出1molH2时转移了2mol电子,发生转移的电子数为2NA,故C正确;
D.没有告诉0.5mol/L MgCl2溶液的体积,无法计算溶液中氯离子的数目,故D错误;
故选AC.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项D为易错点,注意缺少溶液的体积.

练习册系列答案
相关题目
下列说法正确的是( )


| A、图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B、图Ⅱ装置可验证非金属性:Cl>C>Si |
| C、图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D、图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |
下列物质中各含有少量杂质,能用饱和Na2CO3溶液并借助于分液漏斗除去杂质的是( )
| A、苯中含有少量甲苯 |
| B、乙醇中含少量乙酸 |
| C、乙酸乙酯中含有少量乙酸 |
| D、溴苯中含有少量苯 |
丙烯酸(CH3COOCH2-CH=CH-COOH)的性质可能有( )①加成反应 ②水解反应 ③酯化反应 ④中和反应 ⑤氧化反应 ⑥取代反应.
| A、只有①③ |
| B、只有①③④ |
| C、只有①③④⑤ |
| D、①②③④⑤⑥ |
化学来源于生活,应用于生活,渗透在生活的各个领域.下列有关物质的性质与应用的说法不相对应的是( )
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、FeCl3溶液能与铜反应,可用于蚀刻印刷电路板 |
| C、碳酸氢钠可与盐酸反应,可用作抗酸药 |
| D、SiO2具有良好的导电性,可用作光导纤维 |
下列物质中,只含共价键的是( )
| A、KCl |
| B、H2O2 |
| C、NaOH |
| D、CaCl2 |
下列措施中,能加快化学反应速率的是( )
| A、将食物储存在冰箱里 |
| B、用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 |
| C、往H2O2溶液中加入少量MnO2 |
| D、用纯锌代替粗锌与1mol/L H2SO4溶液反应 |
下列叙述不正确的是( )
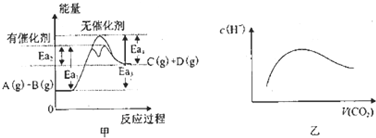

| A、由甲可知,A与B在有催化剂存在的热化学方程式为:A(g)+B(g)?C(g)+D(g)△H═+(Ea3-Ea4)KJ?mol-1 | ||||
B、常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图乙变化关系;当
| ||||
| C、己知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为5.6×10-5mol/L,则生成沉淀所需Na2CO3溶液的最小浓度为2×10-4mol/L | ||||
| D、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混台后(不考虑混台后溶液体积的变化)恰好完全反应,反应后的溶掖中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.05mol?L-1 |
关于元素周期表,以下说法错误的是( )
| A、计算机芯片的组成元素位于第14列 |
| B、元素周期表共有7个周期,16个族 |
| C、每一周期的元素都是从碱金属开始,最后以稀有气体结束 |
| D、第二、三周期中,同一列上下相邻元素的原子核外电子数相差8个 |