题目内容
化学来源于生活,应用于生活,渗透在生活的各个领域.下列有关物质的性质与应用的说法不相对应的是( )
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、FeCl3溶液能与铜反应,可用于蚀刻印刷电路板 |
| C、碳酸氢钠可与盐酸反应,可用作抗酸药 |
| D、SiO2具有良好的导电性,可用作光导纤维 |
考点:盐类水解的应用,硅和二氧化硅,药物的主要成分和疗效
专题:化学应用
分析:A、明矾中铝离子水解生成的Al(OH)3胶体具有吸附性;
B、铁离子具有氧化性把铜氧化而溶解;
C、碳酸氢钠能中和过多的胃酸;
D、SiO2不具有导电性,有导光性.
B、铁离子具有氧化性把铜氧化而溶解;
C、碳酸氢钠能中和过多的胃酸;
D、SiO2不具有导电性,有导光性.
解答:
解:A、明矾中铝离子水解生成的Al(OH)3胶体具有吸附性,可以吸附水中的悬浮颗粒达到净水的目的,故A正确;
B、铁离子具有氧化性把铜氧化而溶解,所以FeCl3溶液可用于蚀刻印刷电路板,故B正确;
C、碳酸氢钠碱性很弱,对人体的刺激较小,碳酸氢钠能中和过多的胃酸,所以可用作抗酸药,故C正确;
D、SiO2不具有导电性,二氧化硅晶体具有导光性,可用作光导纤维,故D错误.
故选:D.
B、铁离子具有氧化性把铜氧化而溶解,所以FeCl3溶液可用于蚀刻印刷电路板,故B正确;
C、碳酸氢钠碱性很弱,对人体的刺激较小,碳酸氢钠能中和过多的胃酸,所以可用作抗酸药,故C正确;
D、SiO2不具有导电性,二氧化硅晶体具有导光性,可用作光导纤维,故D错误.
故选:D.
点评:本题考查了常见物质的性质与用途,主要考查了盐的水解、三价铁离子的性质、碳酸氢钠的性质、二氧化硅的用途,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍.下列说法中不正确的是( )
| A、W、M的某种单质可作为水处理中的消毒剂 |
| B、电解YW2的熔融物可制得Y和W的单质 |
| C、相同条件下,W的氢化物水溶液酸性比Z弱 |
| D、X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
下列说法不正确的是( )
| A、吸热反应不一定需要加热就能发生 |
| B、放热反应在常温下一定很容易发生 |
| C、放热反应有可能也需要加热才能发生 |
| D、反应是放热还是吸热要由反应物和生成物所具有的总能量来决定 |
 反应aA(g)+bB(g)?cC(g)△H=-Q,生成物C的质量分数与压强P和温度T的关系如图,方程式中的系数和Q值符合图象的是( )
反应aA(g)+bB(g)?cC(g)△H=-Q,生成物C的质量分数与压强P和温度T的关系如图,方程式中的系数和Q值符合图象的是( )| A、a+b<c Q>0 |
| B、a+b>c Q<0 |
| C、a+b<c Q<0 |
| D、a+b=c Q>0 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温常压下,9gH2O含有分子数为0.5NA |
| B、标准状况下,以任意比例混合的甲烷和丙烷(C3H8)的气体混合物11.2L,则所含有的分子数为NA |
| C、常温常压下,活泼金属从盐酸中置换出1molH2时发生转移的电子数为2NA |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
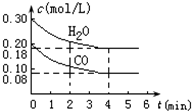 在体积为10L的容器中,通入一定量的CO和H2O,在850℃发生如下反应
在体积为10L的容器中,通入一定量的CO和H2O,在850℃发生如下反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.
CO和H2O浓度变化如图所示;在t℃(高于850℃)时,在相同容器发生上述反应,容器内各物质的浓度如下表:下列叙述不正确的是( )
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | C |
| A、由图可知,0~4 min间平均反应速率v(CO)=0.03mol/(L?min) |
| B、表中3~4 min之间反应处于平衡状态 |
| C、表中3~4 min之间,C1数值小于0.08 mol/L |
| D、表中反应在4~5min间,平衡向逆方向移动的原因可能是增大H2的浓度 |
可逆反应2NO2?O2+2NO在密闭容器中反应,达到平衡状态的标志是( )
| A、NO2、NO和O2 三者共存 |
| B、单位时间内生成2mol NO同时消耗2mol NO2 |
| C、v(NO2)正=2v(O2)逆 |
| D、容器中的各物质物质的量浓度之比为2:2:1的状态 |