题目内容
不能用金属跟盐酸反应直接得到的盐是( )
| A、AlCl3 |
| B、FeCl3 |
| C、MgCl2 |
| D、ZnCl2 |
考点:常见金属元素的单质及其化合物的综合应用
专题:几种重要的金属及其化合物
分析:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,氢离子氧化性弱和变价金属反应只能上传低价的盐,据此进行分析解答.
解答:
解:A、铝的位置排在氢的前面,能与盐酸反应,能生成氯化铝,故A不符合;
B、铁的位置排在氢的前面,可以与盐酸反应,铁与盐酸发生置换反应时生成氯化亚铁,不能生成氯化铁,故B符合;
C、镁的位置排在氢的前面,能与盐酸反应生成氯化镁,故C不符合;
D、锌的位置排在氢的前面,能与盐酸反应生成氯化锌,故D不符合;
故选:B.
B、铁的位置排在氢的前面,可以与盐酸反应,铁与盐酸发生置换反应时生成氯化亚铁,不能生成氯化铁,故B符合;
C、镁的位置排在氢的前面,能与盐酸反应生成氯化镁,故C不符合;
D、锌的位置排在氢的前面,能与盐酸反应生成氯化锌,故D不符合;
故选:B.
点评:本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在,注意变价金属和稀酸反应生成低价盐.

练习册系列答案
相关题目
用铜锌合金制成的黄铜制品常被误作黄金.下列方法不能区分其真伪的是( )
| A、观察外表 | B、放入硝酸中 |
| C、测定密度 | D、放入盐酸中 |
室温时,0.1mol?L-1的HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当滴入少量的NaOH,促进了HA的电离,溶液的pH增大 |
| C、当恰好完全中和时,溶液呈中性 |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
下列离子方程式正确的是( )
| A、氮化镁投入过量盐酸 Mg3N2+6H+═3Mg2++2NH3↑ |
| B、用硫氰化钾溶液检验溶液中的Fe3+:Fe3++3SCN-═Fe(SCN)3↓ |
| C、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| D、硫酸铜溶液中滴加过量的氨水:Cu2++2 NH3?H2O═Cu(OH)2↓+2NH4+ |
如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )


| A、Y、R两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 |
| B、简单离子的半径:X>Z>M |
| C、由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D、Z单质不能从M与R元素构成的盐溶液中置换出单质M |
下列说法一定正确的是( )
| A、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| B、对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
| C、将FeCl3溶液加热蒸干,可得到FeCl3固体 |
| D、0.10mol/L Al2(SO4)3溶液中Al3+数小于0.2NA(NA代表阿伏加德罗常数) |
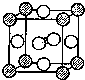 X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素.
X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素. 表示,镍原子用
表示,镍原子用 表示,镁原子用
表示,镁原子用 表示),则该晶体的化学式:
表示),则该晶体的化学式: 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和