题目内容
18.从环己烷可制备1,4-环己二醇的二醋酸酯,下面是有关的8步反应(其中所有无机产物都已略去):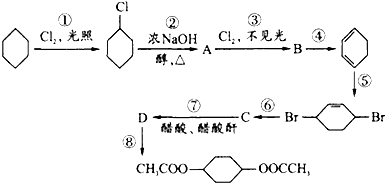
(1)反应①、⑥和⑦属于取代反应.
(2)化合物的结构简式是B
 ,C
,C .
.(3)反应④所用的试剂和条件是浓氢氧化钠、醇、加热.
分析  在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 ,以此来解答.
,以此来解答.
解答 解: 在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 .
.
(1)故①为取代反应,②为消去反应,③为加成反应,④为消去反应,⑤为加成反应,⑥为取代反应,⑦为取代反应,故答案为:⑥;⑦;
(2)由上述分析可知,B的结构简式为 ,C的结构简式为
,C的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
(3) 发生消去反应生成
发生消去反应生成 的反应条件是浓氢氧化钠、醇、加热,故答案为:浓氢氧化钠、醇、加热.
的反应条件是浓氢氧化钠、醇、加热,故答案为:浓氢氧化钠、醇、加热.
点评 本题考查有机物的合成,为高频考点,把握有机合成流程中的官能团变化、有机反应为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
9.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号).原子结构示意图为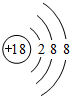 .
.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的名称是KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的氧化物与氢氧化钠反应的化学方程式Al2O3+2OH-=2AlO2-+H2O.
(4)元素④与⑦的化合物属于离子(填“共价”或“离子”)化合物.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的名称是KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的氧化物与氢氧化钠反应的化学方程式Al2O3+2OH-=2AlO2-+H2O.
(4)元素④与⑦的化合物属于离子(填“共价”或“离子”)化合物.
13.下列说法错误的是( )
| A. | H2O比H2S稳定,是因为H2O分子间存在氢键 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | I的原子半径大于Br,HBr比HI的热稳定性强 |
10.A、B、C、D、E 是同一短周期的五种元素,A和B的最高价氧化物对应的水化物呈碱性,且碱性前者强于后者,C和D的最高价氧化物对应的水化物溶液呈酸性,且酸性前者强于后者,五种元素形成的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序是( )
| A. | B A D C E | B. | E C D A B | C. | A B E D C | D. | C D E B A |
8.某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )


| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b连接时,铜片上发生氧化反应 |
 ;
; ;
; ;
; .
.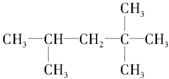 :2,2,4三甲基-戊烷;
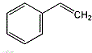
:2,2,4三甲基-戊烷; :间甲基苯乙烯.
:间甲基苯乙烯.