题目内容
下列反应的离子方程式书写正确的是( )
| A、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、氢氧化钡溶液与稀 H2SO4 反应生成硫酸钡沉淀和水;
B、铁和稀硫酸反应生成硫酸亚铁和氢气;
C、铁和铜离子反应生成铜和亚铁离子;
D、碳酸钙难溶于水不能拆成离子.
B、铁和稀硫酸反应生成硫酸亚铁和氢气;
C、铁和铜离子反应生成铜和亚铁离子;
D、碳酸钙难溶于水不能拆成离子.
解答:
解:A、氢氧化钡溶液与稀 H2SO4 反应生成硫酸钡沉淀和水,反应的离子方程式Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A错误;
B、铁和稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式:Fe+2H+=Fe2++H2↑,故B错误;
C、铁和铜离子反应生成铜和亚铁离子,反应的离子方程式为:Cu2++Fe=Fe2++Cu,故C正确;
D、碳酸钙难溶于水不能拆成离子,反应的离子方程式为:CaCO3+2H+=H2O+CO2↑+Ca2+,故D错误;
故选C.
B、铁和稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式:Fe+2H+=Fe2++H2↑,故B错误;
C、铁和铜离子反应生成铜和亚铁离子,反应的离子方程式为:Cu2++Fe=Fe2++Cu,故C正确;
D、碳酸钙难溶于水不能拆成离子,反应的离子方程式为:CaCO3+2H+=H2O+CO2↑+Ca2+,故D错误;
故选C.
点评:本题考查了离子方程式书写方法和注意问题,注意量不同产物不同的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+4OH-═Y+S4O62-+2H2O,下列有关说法正确的是( )
| A、Y的化学式为Fe2O3 |
| B、S4O62-是还原产物 |
| C、被1mol O2氧化的Fe2+物质的量为1mol |
| D、每 32 gO2参加反应,转移电子的物质的量为4mol |
2003年诺贝尔物理学奖颁给三位对超导和超流理论方面进行研究并作出先驱性贡献的科学家.低温液态的42He和32He具有超流体特性.关于42He说法错误的是( )
| A、质子数为2 |
| B、电子数为2 |
| C、质量数为4 |
| D、中子数为4 |
下列根据反应原理设计的应用,不正确的是( )
| A、CO32-+H2O?HCO3-+OH-实验室盛放Na2CO3溶液的试剂瓶应用橡皮塞,而不用玻璃塞 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、2SbCl3+3H2O?Sb2O3+6HCl实验室可利用SbCl3的水解反应制取Sb2O3 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
下列化学方程式或离子方程式正确的是( )
A、苯酚钠溶液中通入少量二氧化碳的离子方程式: |
B、制备酚醛树脂的化学方程式: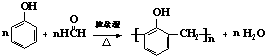 |
C、丙烯聚合成聚丙烯的化学方程式: |
| D、丙烯与溴化氢主反应为:CH3-CH=CH2+HBr→CH3-CH2-CHBr |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、NA个氧分子与NA个氢分子的质量比是16:1 |
| B、18克水所含电子数为NA |
| C、19.6g硫酸所含的硫原子数为0.1 NA |
| D、2.4g镁变成镁离子时,失去电子数目为0.1 NA |
下列变化过程中△H<0的是( )
| A、电解Al2O3得到Al和O2 |
| B、HCl分解为H2和Cl2 |
| C、焦碳与水蒸气反应 |
| D、Na与水反应 |