题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、NA个氧分子与NA个氢分子的质量比是16:1 |
| B、18克水所含电子数为NA |
| C、19.6g硫酸所含的硫原子数为0.1 NA |
| D、2.4g镁变成镁离子时,失去电子数目为0.1 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.含NA个微粒的物质的物质的量为1mol,依据m=n×M分别求出1mol氧气和1mol氢气的质量以此解答;’
B.利用n=
和水分子为10电子体分析解答;
C.利用n=
求出硫酸的物质的量,依据硫酸分子中硫原子个数计算;
D.利用n=
求出镁的物质的量,结合Mg→Mg2+失去2个电子解答.
B.利用n=
| m |
| M |
C.利用n=
| m |
| M |
D.利用n=
| m |
| M |
解答:
解:A.NA个氧分子物质的量为1mol,所以氧气的质量为m(O2)=1mol×32g/mol=32g;
NA个氢分子物质的量为1mol,所以氢气的质量为m(H2)=1mol×2g/mol=2g;
则二者质量之比=32g:2g=16:1,故A正确;
B.18克水物质的量为
=1mol,所含电子数为1mol×10×NA=10NA,故B错误;
C.19.6g硫酸的物质的量为
=0.2mol,一个硫酸分子中含有一个硫原子,所以硫原子的个数为:0.2mol×1×NA=0.2NA,故C错误;
D.2.4g镁物质的量为
=0.1mol,Mg→Mg2+失去2个电子,所以失去电子数目为:0.1mol×2×NA=0.2NA,故D错误;
故选A.
NA个氢分子物质的量为1mol,所以氢气的质量为m(H2)=1mol×2g/mol=2g;
则二者质量之比=32g:2g=16:1,故A正确;
B.18克水物质的量为
| 18g |
| 18g/mol |
C.19.6g硫酸的物质的量为
| 19.6g |
| 98g/mol |
D.2.4g镁物质的量为
| 2.4g |
| 24g/mol |
故选A.
点评:阿伏伽德罗是高考必考题,题目难度不大,抓住微粒数目、质量、体积、浓度、物质的量的关系是解题的关键.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下图所示.下列说法正确的是
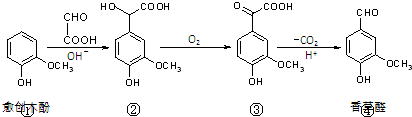 ( )
( )
 ( )
( )| A、在上述三步反应中理论上只有①生成②的反应原子利用率为100% |
| B、氯化铁溶液和碳酸氢钠溶液都能鉴别③④ |
| C、②分子中C原子不可能在同一平面上 |
| D、等物质的量的①②分别与足量NaOH溶液反应,消耗NaOH的物质的量之比为1:3 |
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等同属于离子型碳化物,已知CaC2+2H2O→C2H2↑+Ca(OH)2请通过对CaC2制C2H2的反应原理进行思考,从中得到启示,判断下列产物正确的是( )
| A、Mg2C3水解生成丙炔(C3H4) |
| B、ZnC2水解生成C2H4 |
| C、Li2C2水解生成C2H4 |
| D、Al4C3水解生成甲烷CH4 |
下列说法正确的是( )
A、按系统命名法,有机物 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 |
| B、将1-溴丙烷和饱和氢氧化钾乙醇溶液共热,产生的气体通过酸性高锰酸钾溶液,溶液褪色,一定能证明1-溴丙烷发生了消去反应 |
C、纤维素  和壳聚糖 和壳聚糖 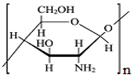 均属于多糖 均属于多糖 |
D、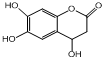 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
下列叙述错误的是( )
| A、某溶液中加入Ba(NO3)2溶液和稀盐酸(过量)析出白色沉淀,则溶液中一定含SO42- |
| B、硫酸加入漂白粉中能生成氯气,可用排饱和食盐水法收集 |
| C、NaOH溶液不能保存在带胶头滴管的试剂瓶中,因为NaOH与磨口处的SiO2反应生成Na2SiO3形成粘结 |
| D、可用热的饱和碳酸钠溶液除去金属表面的植物油 |
将一小块钠投入滴有石蕊的水中,下列有关现象的叙述错误的是( )
| A、钠浮在液面上 |
| B、有无色无味的气体产生 |
| C、水溶液变为蓝色 |
| D、水溶液变为红色 |
只用一种试剂,就能把Na2S、Ba(NO3)2、NaHCO3、AlCl3、NaAlO2五种无色透明溶液区别开来,这种试剂是( )
| A、硫酸 | B、盐酸 |
| C、氨水 | D、氢氧化钠溶液 |