题目内容
10.(1)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.①若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,原因是锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀.
②MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式2H++2e=H2↑.
(2)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2═4LiCl+S+SO2.请回答下列问题:电池的负极材料为锂,电池正极发生的电极反应为2SOCl2+4e-=4Cl-+S+SO2.
(3)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在650℃下工作的燃料电池,完成有关电池反应式.阳极反应式:2CO+2CO32--4e-═4CO2,阴极反应式:O2+2CO2+4e-=2CO32-.
(4)电解饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,电解池中阳极上的电极反应式为2Cl--2e-=Cl2↑.在阴极附近观察到的现象是有无色气体生成,同时溶液变红色.
分析 (1)①锌与杂质铜离子发生氧化还原反应,生成铜与锌构成原电池;
②阴极是氧化性强的氢离子发生还原反应生成氢气;
(2)由反应4Li+2SOCl2═4LiCl+S+SO2分析反应的化合价变化,可得Li为还原剂,SOCl2为氧化剂,负极材料为Li(还原剂),发生氧化反应,电极反应式为Li-e-═Li+,正极发生还原反应,电极方程式为:2SOCl2+4e-═4Cl-+S+SO2,据此分析;
(3)阴极氧气发生还原反应生成氧负离子,结合二氧化碳,生成碳酸根离子,电极反应式为:O2+2CO2+4e-=2CO32-;
(4)电解池中阳极上氯离子发生氧化反应,阳极的电极反应式为2Cl--2e-=Cl2↑,在阴极水电离的氢离子放电生成氢气,产生氢氧根离子,使溶液呈碱性.
解答 解:(1)①锌与杂质铜离子发生氧化还原反应,生成铜与锌构成原电池,所以反应速率加快,故答案为:锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀;
②阴极是氧化性强的氢离子发生还原反应生成氢气,所以电极反应式为:2H++2e=H2↑,故答案为:2H++2e=H2↑;
(2)由反应4Li+2SOCl2═4LiCl+S+SO2分析反应的化合价变化,可得Li为还原剂,SOCl2为氧化剂,负极材料为Li(还原剂),发生氧化反应,电极反应式为Li-e-═Li+,正极发生还原反应,电极方程式为:2SOCl2+4e-═4Cl-+S+SO2,故答案为:锂; 2SOCl2+4e-=4Cl-+S+SO2;
(3)阴极氧气发生还原反应生成氧负离子,结合二氧化碳,生成碳酸根离子,电极反应式为:O2+2CO2+4e-=2CO32-,故答案为:O2+2CO2+4e-=2CO32-;
(4)电解池中阳极上氯离子发生氧化反应,阳极的电极反应式为2Cl--2e-=Cl2↑,在阴极水电离的氢离子放电生成氢气,产生氢氧根离子,使溶液呈碱性,所以观察到有无色气体生成,同时溶液变红色,故答案为:2Cl--2e-=Cl2↑;有无色气体生成,同时溶液变红色.
点评 本题以燃料电池为载体考查原电池原理,侧重考查学生书写电极反应式,注意结合电解质书写电极反应式,为学习难点.

| A. | 蔗糖与纤维素均属于高分子化合物 | |
| B. | 不同的油脂发生皂化反应,至少有一种产物相同 | |
| C. | 淀粉在稀硫酸作用下充分加热后,所得溶液与少量新制Cu(OH)2共热未见红色沉淀,说明淀粉未发生水解 | |
| D. | 蛋白质溶液中加入酒精后会发生盐析而失去生理活性 |
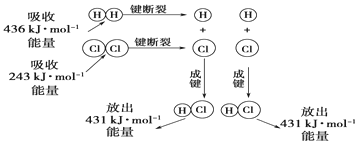
| A. | -332kJ | B. | -118kJ | C. | +130kJ•mol-1 | D. | +350kJ•mol-1 |
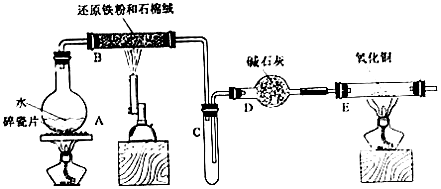
(1)烧瓶底部放置了几片碎瓷片,碎资片的作用是防暴沸.装置B中发生反应的化学方程式是3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4.
(2)如果要在E处玻璃管处点燃该气体,则必须对该气体进行验纯装置中的现象是黑色变为紫红色,试管口有水珠生成..
(3)将探究小组分为两组,按题图装置进行对比实验,甲组用洒精喷灯、乙组用洒精灯加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验.
| 步骤 | 操作 | 甲组现象 | 乙组现象 | |
| 1 | 取黑色粉末加入稀盐酸 | 洛解,无气泡 | 溶解,无气泡 | |
| 2 | 取少骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 | |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 | |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 | |
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Cl2+2Fe2+=2Fe3++2Cl-,Fe3++SCN-=FeSCN2+;溶液褪色可能的原因是氯水将SCN-氧化破坏了;验证方法为继续向溶液中滴入KSCN溶液,溶液变红即可证明.
(4)其中一组同学将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL.5mol•L-1FeSO4溶液和5.2g固体沉淀物,则原Fe2(SO4)3溶液的物质的量浓度为0.1mol/L;将沉淀物过滤后,该组同学又向清液中滴加稀硝酸,观察到有NO气体生成,发生的化学反应方程式为6FeSO4+8HNO3=2Fe2(SO4)3+2NO↑+4H2O+2Fe(NO3)3.
| A. | 除去乙烷中少量的乙烯:气体通过盛酸性高锰酸钾溶液的洗气瓶 | |
| B. | 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤、分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰、蒸馏 |
 亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:①2NO+Na2O2═2NaNO2
②2NO2+Na2O2═2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-被还原成Mn2+.
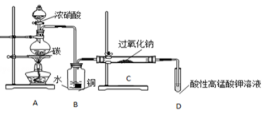
Ⅰ.产品制备与检验:用如图装置制备NaNO2
(1)写出装置A烧瓶中发生反应的化学方程式C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO);盛浓硝酸的仪器名称为分液漏斗.
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管.在干燥管中盛放的试剂名称为碱石灰.
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,滴加少量酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.