��Ŀ����
18��ijУ��ѧ�ס�������С��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ��������ʡ���ʵ�飮��ͼ�мгּ�β������װ�þ�����ȥ��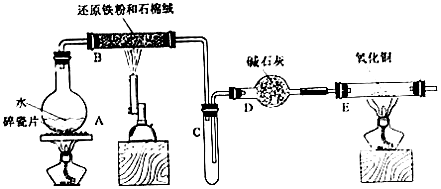
��1����ƿ�ײ������˼�Ƭ���Ƭ������Ƭ�������Ƿ����У�װ��B�з�����Ӧ�Ļ�ѧ����ʽ��3Fe+4H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$4H2+Fe3O4��
��2�����Ҫ��E�������ܴ���ȼ�����壬�����Ը���������鴿װ���е������Ǻ�ɫ��Ϊ�Ϻ�ɫ���Թܿ���ˮ�����ɣ���
��3����̽��С���Ϊ���飬����ͼװ�ý��жԱ�ʵ�飬������������ơ������������Ƽ��ȣ���Ӧ�����Ϊ��ɫ��ĩ�������������ֱ��ò����������ʵ�飮
| ���� | ���� | �������� | �������� | |
| 1 | ȡ��ɫ��ĩ����ϡ���� | ��⣬������ | �ܽ⣬������ | |
| 2 | ȡ����1����Һ���μ�����KMnO4��Һ | ��ɫ��ȥ | ��ɫ��ȥ | |
| 3 | ȡ����1����Һ���μ�KSCN��Һ | ��� | ������ | |
| 4 | ����3��Һ�еμ�������ˮ | ��ɫ��ȥ | �ȱ�죬����ɫ | |
�ڼ��鲽��1�з�Ӧ�����ӷ���ʽΪFe3O4+8H+=2Fe3++Fe2++4H2O��
�����鲽��4�У���Һ����ԭ��ΪCl2+2Fe2+=2Fe3++2Cl-��Fe3++SCN-=FeSCN2+����Һ��ɫ���ܵ�ԭ������ˮ��SCN-�����ƻ��ˣ���֤����Ϊ��������Һ�е���KSCN��Һ����Һ��켴��֤����
��4������һ��ͬѧ��6g���ۼ���200mLFe2��SO4��3��CuSO4�Ļ����Һ�У���ַ�Ӧ�õ�200mL.5mol•L-1FeSO4��Һ��5.2g����������ԭFe2��SO4��3��Һ�����ʵ���Ũ��Ϊ0.1mol/L������������˺���ͬѧ������Һ�еμ�ϡ���ᣬ�۲쵽��NO�������ɣ������Ļ�ѧ��Ӧ����ʽΪ6FeSO4+8HNO3=2Fe2��SO4��3+2NO��+4H2O+2Fe��NO3��3��
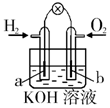
���� A�ṩˮ������B��ˮ��������������Ӧ3Fe+4H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$4H2+Fe3O4��CΪ�������ռ�װ�ã�DΪ����װ�ã�E������������ͭ��Ӧ����ͭ��ˮ��
��1�����ȴ�Һ��Ӧ��ֹ���У�����ˮ������Ӧ����������������������
��2�������ڵ�ȼʱӦ���鴿������������ͭ�����û���Ӧ��
��3���������������ڼ���KSCN����죬˵�����������ӣ�������������ܽ�ֱ����KSCN��죬˵�����������ӣ�������������ɫ��˵�������������ӣ�����ʵ��μ���ˮ�������ֺ�ɫ��ȥ����˵����������SCN-��
��4����������Fe3+��Cu2+����������ۣ��ȷ���Fe+Fe2 ��SO4��3=3FeSO4��5.2g���������һ����ͭ�������Fe+CuSO4=FeSO4+Cu��Ȼ����ݻ�ѧ��Ӧ����ʽ���ɼ��㣻����ͬѧ������Һ�еμ�ϡ���ᣬ�۲쵽��NO�������ɣ�˵�����������������ӣ�
��� �⣺��1�����ȴ�Һ��ʱ�������Ƭ���ɷ�ֹ���У�����ˮ������Ӧ��������������������������ʽΪ3Fe+4H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$4H2+Fe3O4��
�ʴ�Ϊ�������У�3Fe+4H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$4H2+Fe3O4��
��2�������ڵ�ȼʱӦ���鴿����ֹ������������ը������������ͭ�����û���Ӧ���ɹ۲쵽��ɫ��Ϊ�Ϻ�ɫ�����Թܿ���ˮ�����ɣ�
�ʴ�Ϊ���鴿����ɫ��Ϊ�Ϻ�ɫ���Թܿ���ˮ�����ɣ�
��3�����������������ڼ���KSCN����죬˵�����������ӣ������ɺ�ɫ����ΪFeO���ʴ�Ϊ��FeO��
�ڼ�����������ܽ�ֱ����KSCN��죬˵�����������ӣ�������������ɫ��˵�������������ӣ�˵����������Fe3O4���������ᣬ����Fe3O4+8H+=2Fe3++Fe2++4H2O��
�ʴ�Ϊ��Fe3O4+8H+=2Fe3++Fe2++4H2O��
�����鲽��4������ˮ������Cl2+2Fe2+=2Fe3++2Cl-��KSCN�������ӷ���Fe3++SCN-=FeSCN2+������ʵ��μ���ˮ�������ֺ�ɫ��ȥ����˵����������SCN-������֤���ɼ�������Һ�е���KSCN��Һ����Һ��켴��֤����
�ʴ�Ϊ��Cl2+2Fe2+=2Fe3++2Cl-��Fe3++SCN-=FeSCN2+����ˮ��SCN-�����ƻ��ˣ���������Һ�е���KSCN��Һ����Һ��켴��֤����
��4����Һ�к���Fe2+��0.5mol•L-1��0.2L=0.1mol��$\frac{6g}{56g/mol}$��
��6g���۹������跴Ӧ�����������ʵ���Ϊx������ͭ�����ʵ���Ϊy��
Fe+Fe2 ��SO4��3=3FeSO4
1mol 1mol 3mol
xmol xmol 3xmol
Fe+CuSO4=FeSO4+Cu
1mol 1mol 1mol 1mol
ymol ymol ymol ymol
�ɵ�$\left\{\begin{array}{l}{3x+y=0.1mol}\\{6g-56x+64y=5.2}\end{array}\right.$��
���x=0.02mol��y=0.04mol��
ԭ��Һ��Fe2��SO4��3���ʵ���Ũ��Ϊ$\frac{0.02mol}{0.2L}$=0.1mol/L��
����ͬѧ������Һ�еμ�ϡ���ᣬ�۲쵽��NO�������ɣ�˵�����������������ӣ�����ʽΪ6FeSO4+8HNO3=2Fe2��SO4��3+2NO��+4H2O+2Fe��NO3��3��
�ʴ�Ϊ��0.1mol/L�� 6FeSO4+8HNO3=2Fe2��SO4��3+2NO��+4H2O+2Fe��NO3��3��
���� ���⿼�����ʵ�����ʵ�飬���ؿ��������ӡ��������ӵļ��鷽��������ʵ�鷽������������ۣ�Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ������ۺ��Խ�ǿ��ע����ȷ���⡢����������Ϣ����ϵ��ѧ��֪ʶ���н��

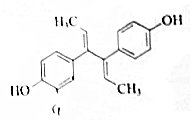 ˫ϩ�Ʒ����˹��ϳɵĴƼ��ػ������ṹ��ʽ��ͼ������˵������ȷ���ǣ�������
˫ϩ�Ʒ����˹��ϳɵĴƼ��ػ������ṹ��ʽ��ͼ������˵������ȷ���ǣ�������| A�� | ����ʽΪC18H18O2���������ȷ»�����������Һ | |
| B�� | ˫ϩ�ƷӼȿɷ����Ӿ۷�Ӧ��Ҳ���Է������۷�Ӧ | |
| C�� | �䱽���ϵĶ��ȴ�����7�� | |
| D�� | 1 mol˫ϩ�ƷӸ�H2��Ӧ����������8mol H2�� |
| A�� | �۱�ϩ�����ڣ�-CH2CH��CH3��- | B�� | ����ķ���ʽ��CH3COOH | ||
| C�� | ���������ӵĽṹ��ʽ��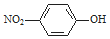 | D�� | H2S�ĵ���ʽ�� |
| A�� | �ñ���ʳ��ˮ���ˮ����ʯ���ã�������Ч���Ʋ�����Ȳ������ | |
| B�� | �Ʒ���ʱ��������Һ����뱥��ʳ��ˮ���ܹ��ٽ���֬�����Ƶ����� | |
| C�� | �Ʊ���������ʱ��Ϊ��ȥ���������е����ᣬ�ñ���̼������Һ�ռ����� | |
| D�� | ����ϩʱ��������Ϊ100����¶ȼƴ�������Ϊ300����¶ȼƣ��ⷴӦҺ���¶� |
| A�� | ������0.1 mol/L��������Һ��NH4Al��SO4��2 ��NH3•H2O ��NH4Cl ��CH3COONH4�У�c��NH4+���ɴ�С��˳���ǣ��٣��ۣ��ܣ��� | |
| B�� | ����ʱ��pH=4��HCOOH��Һ��pH=10�İ�ˮ�������ϣ�pH=4��H2SO4��Һ��pH=10��NaOH��Һ�������ϣ��������Һ����ˮ�����c��H+��һ������� | |
| C�� | ������0.4mol/L HB��Һ��0.2mol/L NaOH��Һ�������Ϻ����Ϻ���Һ������Ũ�ȵĴ�С˳��һ��Ϊ��c��B-����c��Na+����c��H+����c��OH-�� | |
| D�� | ������0��lmol/L pHΪ4��NaHA��Һ�У�c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� |
| A | B | C | D |
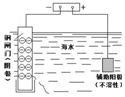
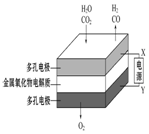
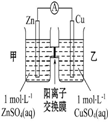
| ��բ�����ױ���ʴ | a��b��Ϊ���Ե缫��b����Ӧ�ǣ�O+4OH--4e-=2H2O | �������������ɵ���������ʵ���֮����1��1 | ��ع���һ��ʱ�� ���ҳ���Һ������������ |
 |  |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
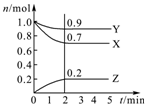 ij�¶�ʱ����2L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã�
ij�¶�ʱ����2L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã�