��Ŀ����
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����

��1��ͼ1�DZ�ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾƽ����Ӧ����v��CO��= �� H2��ƽ��ת����Ϊ ��
��2��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯��д����Ӧ���Ȼ�ѧ����ʽ ��
��3�����¶��£���Ӧƽ�ⳣ��K= ������ֵ�����¶����ߣ�ƽ�ⳣ��K ������������䡱��С������
��4�����������£����д�ʩ����ʹ��Ӧ��ϵ��
����Ĵ�ʩ�� ��
a�������¶� b������He�� c���ٳ���2molH2 d��ʹ�ô�����

��1��ͼ1�DZ�ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾƽ����Ӧ����v��CO��=
��2��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯��д����Ӧ���Ȼ�ѧ����ʽ
��3�����¶��£���Ӧƽ�ⳣ��K=
��4�����������£����д�ʩ����ʹ��Ӧ��ϵ��
| n(CH3OH) |
| n(CO) |
a�������¶� b������He�� c���ٳ���2molH2 d��ʹ�ô�����
���㣺���ʵ�����Ũ����ʱ��ı仯����,��ѧƽ���Ӱ������
ר�⣺��ѧƽ��ר��
��������1������v=
���㣬�ɵ÷�Ӧ���ʣ�����ת����=
��100%�����ת���ʣ�
��2�����ݷ�Ӧ��������������������������Ȼ��Ƿ��ȣ�����д�Ȼ�ѧ��Ӧ����ʽ��
��3����ѧƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��ݴ����ƽ�ⳣ���������¶ȶԻ�ѧƽ���Ӱ��������ƽ�ⳣ���ı仯��
��4��ʹ
������ѧƽ��Ӧ�����ƶ����ݴ��жϣ�
| ��c |
| t |
| ��ת�������ʵ��� |
| ��ʼ�����ʵ��� |
��2�����ݷ�Ӧ��������������������������Ȼ��Ƿ��ȣ�����д�Ȼ�ѧ��Ӧ����ʽ��
��3����ѧƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��ݴ����ƽ�ⳣ���������¶ȶԻ�ѧƽ���Ӱ��������ƽ�ⳣ���ı仯��
��4��ʹ
| n(CH3OH) |
| n(CO) |
���
�⣺��1����ͼ��֪��COŨ�ȱ仯��Ϊ1.00mol/L-0.25mol/L=0.75mol/L����t=10min����v��CO��=
=0.075mol/��L?min����
��COŨ�ȱ仯��Ϊ0.75mol/L�����ݻ�ѧ����ʽ��֪H2Ũ�ȱ仯��Ϊ1.5mol/L��H2��ƽ��ת����=
��100%=75%��
�ʴ�Ϊ��0.075mol/��L?min����75%��
��2����Ӧ������������ܵIJ�ֵΪ419kJ������������������ܵIJ�ֵΪ510kJ����÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ419kJ-510kJ=91kJ���Ȼ�ѧ����ʽΪCO��g��+2H2��g��=CH3OH��g����H=-91 kJ/mol���ʴ�Ϊ��CO��g��+2H2��g��=CH3OH��g����H=-91 kJ/mol��
��3��H2ƽ��ʱ��Ũ��=2mol/L-1.5mol/L=0.5mol/L���ٽ��ͼ�ã�
CO��g��+2H2��g��?CH3OH��g��
ƽ��ʱ��Ũ�ȣ�mol/L�� 0.25 0.5 0.75
��K=
=
mol-2?L-2=12 mol-2?L-2
��÷�ӦΪ���ȷ�Ӧ���������¶ȣ���ѧƽ�������ƶ�������Kֵ��С��
�ʴ�Ϊ��12����С��
��4��ʹ
����ѧƽ��Ӧ�����ƶ����������¶�ʱ��ѧƽ�������ƶ�����a�����������³���He����ѧƽ�ⲻ�ƶ�����b����ʹ�ô�����ѧƽ�ⲻ�ƶ�����d�����ں����������ٳ���2molH2��ѹǿ����ѧƽ�������ƶ����������⣬��c��ȷ��
�ʴ�Ϊ��c��
| 0.75mol/L |
| 10min |
��COŨ�ȱ仯��Ϊ0.75mol/L�����ݻ�ѧ����ʽ��֪H2Ũ�ȱ仯��Ϊ1.5mol/L��H2��ƽ��ת����=
| 1.5��2 |
| 4 |
�ʴ�Ϊ��0.075mol/��L?min����75%��
��2����Ӧ������������ܵIJ�ֵΪ419kJ������������������ܵIJ�ֵΪ510kJ����÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ419kJ-510kJ=91kJ���Ȼ�ѧ����ʽΪCO��g��+2H2��g��=CH3OH��g����H=-91 kJ/mol���ʴ�Ϊ��CO��g��+2H2��g��=CH3OH��g����H=-91 kJ/mol��
��3��H2ƽ��ʱ��Ũ��=2mol/L-1.5mol/L=0.5mol/L���ٽ��ͼ�ã�
CO��g��+2H2��g��?CH3OH��g��
ƽ��ʱ��Ũ�ȣ�mol/L�� 0.25 0.5 0.75
��K=
| c(CH3OH) |
| c(CO)��c2(H2) |
| 0.75 |
| 0.25��0��52 |
��÷�ӦΪ���ȷ�Ӧ���������¶ȣ���ѧƽ�������ƶ�������Kֵ��С��
�ʴ�Ϊ��12����С��
��4��ʹ
| n(CH3OH) |
| n(CO) |
�ʴ�Ϊ��c��
���������⿼����ѧ���Է�Ӧ�ȵ����⡢ƽ��ת���ʵļ��㡢Ӱ�컯ѧƽ���ƶ������ص�����������Ѷ��еȣ�������һ�����ۺ��ԣ�����ʱҪע�������������Ӧ�ü�������

��ϰ��ϵ�д�
 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д� �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
�����Ŀ
��ѧ��Ԥ�ԣ���ˮ���ý���Ϊһ����̵����Σ������������Ϊ��������
| A��������ˮ���٣����������������Ҫ |
| B������ɳĮ����ʹ������ˮ�������ϼ��� |
| C�����ڵ���������µ����ã�ˮ�ᱻ���������� |
| D����ˮ��Դ�����㣬�ֲ��ֺܲ����ȣ���������ʹˮ���ϵ��ܵ���Ⱦ��ʹ��ˮ��ԴԽ��Խ��ȱ |
�������ӷ���ʽ��ȷ���ǣ�������
| A��������̼������Һ��Ӧ��2H++CO32-�TCO2��+H2O | ||
| B��������Һ������������ͭ��Ӧ��2CH3COOH+Cu��OH��2��Cu2++2CH3COO-+2H2O | ||
C����������Һ��ͨ������������̼��2C6H5O-+CO2+H2O
| ||
D����ȩ��Һ��������������Һ���ȣ�HCHO+4[Ag��NH3��2]++4OH-
|

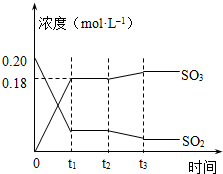 ��֪2SO2 ��g��+O2��g��?2SO3��g����H=-196kJ?mol-1��5000Cʱ��2mol SO2��1molO2װ��һ����㶨��10L�ܱ������У�2���ӣ�t1��ʱ�ﵽƽ�⣮��ͼ��ʾ��
��֪2SO2 ��g��+O2��g��?2SO3��g����H=-196kJ?mol-1��5000Cʱ��2mol SO2��1molO2װ��һ����㶨��10L�ܱ������У�2���ӣ�t1��ʱ�ﵽƽ�⣮��ͼ��ʾ��