题目内容
20.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 标准状况下,22.4 LCCl4含有的分子数为NA | |
| B. | 1L0.1 mol•L-1 Na2CO3溶液中含有CO32-数为0.1 NA | |
| C. | 常温常压下,18g水含有的分子数为 NA | |
| D. | 常温下,1mol Cl2与过量NaOH溶液反应,转移电子总数为2NA |
分析 A、标况下四氯化碳为液态;
B、碳酸根是弱酸根,在溶液中能水解;
C、水分子个数N=$\frac{m}{M}{N}_{A}$;
D、氯气和氢氧化钠的反应为歧化反应.
解答 解:A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、碳酸根是弱酸根,在溶液中能水解,故溶液中含有的碳酸根的个数小于0.1NA个,故B错误;
C、水分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{18g}{18g/mol}{N}_{A}/mol$=NA个,故C正确;
D、氯气和氢氧化钠的反应为歧化反应,故1mol氯气转移1mol电子即NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.有关亚硫酸的下列叙述中,不正确的是( )
| A. | 亚硫酸是SO2与水反应的产物,显酸性 | |
| B. | SO2溶于水,剧烈反应生成亚硫酸 | |
| C. | 亚硫酸具有漂白性,能够使品红溶液褪色 | |
| D. | 亚硫酸不稳定,容易分解为水和SO2 |
8.下列说法不正确的是( )
| A. | pH只适用于稀溶液,对于c(H+)>1 mol/L时,一般不用pH而直接用H+的浓度表示 | |
| B. | 水的电离、弱酸、弱碱的电离及盐类水解都是吸热的 | |
| C. | pH每增加一个单位,c(H+) 则减少10倍 | |
| D. | 25℃纯水中加入盐酸后,pH<7,此时水的离子积常数KW≠1×10-14 |
5.下列说法中正确的是( )
| A. | 氯化钠在电流的作用下电离出Na+和Cl- | |
| B. | CaCO3难溶于水,但CaCO3属于强电解质 | |
| C. | 二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 | |
| D. | 硫酸钠在水中的电离方程式可表示为Na2SO4═2Na++S6++4O2- |
12.网传云南曲靖市越州镇约5000余吨的重毒化工废料铬渣被非法丢放,毒水被直接排放到南盘江中.
I.某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是C13+,其次是Fe3+、Al3+、Ca2+、Mg2+):
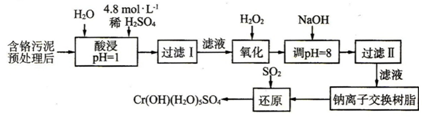
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用18.4mol/L浓硫酸配制250mL 4.8mol/L硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需250mL容量瓶、胶头滴管.
(2)加入H202的作用是氧化+3价Cr使之转变成+6价Cr(或Cr2O72-),以便于与杂质离子分离.调节溶液的pH=8 是为了除去Fe3+和Al3+离子.
(3)还原过程发生以下反应,请配平:
1Na2Cr2O7+3S02+11H2O═2Cr(OH)(H20)5S04+1Na2S04
(4)钠离子交换树脂的原理为Mn++nNaR═MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
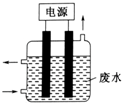
Ⅱ.工业废水中常含有一定量的Cr2O72-和Cr042-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为Fe-2e-=Fe2+.在阴极附近溶液pH升高的原因是2H++2e-=H2 ↑(用电极反应方程式解释).产生的阳极产物在处理废水中铬元素时所起的作用是做还原剂,将+6价的Cr还原为+3价的Cr.
I.某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是C13+,其次是Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | ─ | ─ | 4.7 | ─ |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(2)加入H202的作用是氧化+3价Cr使之转变成+6价Cr(或Cr2O72-),以便于与杂质离子分离.调节溶液的pH=8 是为了除去Fe3+和Al3+离子.
(3)还原过程发生以下反应,请配平:
1Na2Cr2O7+3S02+11H2O═2Cr(OH)(H20)5S04+1Na2S04
(4)钠离子交换树脂的原理为Mn++nNaR═MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
Ⅱ.工业废水中常含有一定量的Cr2O72-和Cr042-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为Fe-2e-=Fe2+.在阴极附近溶液pH升高的原因是2H++2e-=H2 ↑(用电极反应方程式解释).产生的阳极产物在处理废水中铬元素时所起的作用是做还原剂,将+6价的Cr还原为+3价的Cr.
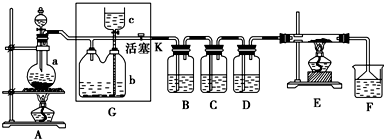
 “8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题:
“8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题: .
.