题目内容
下列有关叙述,正确的是( )
| A、加碘食盐能使淀粉溶液变蓝 |
| B、用电石和水反应制乙炔是氧化还原反应 |
| C、1mol乙酸与足量乙醇在浓硫酸催化下加热,可生成1 mol乙酸乙酯 |
| D、利用电石与水反应制取C2H2时,可采用CuSO4溶液除去杂质气体 |
考点:生活中的有机化合物,有机化学反应的综合应用
专题:有机反应
分析:A.淀粉遇碘变蓝色;
B.凡是有化合价的升降的是氧化还原反应;
C.羧酸与醇的酯化反应是可逆反应;
D.生成的气体含有硫化氢,可与硫酸铜反应.
B.凡是有化合价的升降的是氧化还原反应;
C.羧酸与醇的酯化反应是可逆反应;
D.生成的气体含有硫化氢,可与硫酸铜反应.
解答:
解:A.食盐中的碘为碘酸盐,而淀粉遇碘变蓝色,故A错误;
B.用电石和水反应制乙炔是非氧化还原反应,故B错误;
C.乙酸与乙醇反应生成乙酸乙酯,属于可逆反应,反应物不能完全转化,故C错误;
D.生成的气体含有硫化氢,可与硫酸铜反应生成硫化铜沉淀,可用于除杂,故D正确.
故选D.
B.用电石和水反应制乙炔是非氧化还原反应,故B错误;
C.乙酸与乙醇反应生成乙酸乙酯,属于可逆反应,反应物不能完全转化,故C错误;
D.生成的气体含有硫化氢,可与硫酸铜反应生成硫化铜沉淀,可用于除杂,故D正确.
故选D.
点评:本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构、性质以及用途,难度不大,注意相关基础知识的积累.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,关于铅蓄电池的说法正确的是( )
| A、放电时正极发生的反应是:Pb(s)+SO42-(aq)-2e-═PbSO4(s) |
| B、放电时该电池的负极材料是铅板 |
| C、充电时,阳极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
| D、充电时,电池中硫酸的浓度不断增大 |
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、有碳碳双键、羰基、羧基 |
| B、苯环、羟基、羰基 |
| C、有羰基、羧基、酯基 |
| D、有碳碳双键、苯环、羧基 |
下列操作方法或实验装置正确的是( )
A、 |
B、 |
C、 |
D、 |
两种浓度不同的NaOH溶液,c(H+)分别为1.0×10-14 mol?L-1和1.0×10-12 mol?L-1,将这两种溶液等体积混合后,所得溶液的c(H+)约为( )
| A、0.5×(10-14+10-12) mol?L-1 |
| B、5×(10-15+10-11) mol?L-1 |
| C、2.0×10-1 mol?L-1 |
| D、2.0×10-14 mol?L-1 |
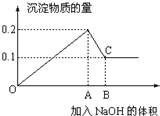 在100mL MgCl2和AlCl3的混和溶液中,逐滴加入1mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则:
在100mL MgCl2和AlCl3的混和溶液中,逐滴加入1mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则: