题目内容
12.下列有关叙述正确的是( )| A. | 电泳现象可证明胶体带电荷 | |
| B. | 直径在1~100mm之间的粒子称为胶体 | |
| C. | 是否具有丁达尔效应是溶液和胶体的本质区别 | |
| D. | 胶体粒子很小,可以透过滤纸 |
分析 A、胶体不带电;
B、胶体属于分散系;
C、溶液、胶体和浊液的本质区别是分散质粒子直径大小;
D、胶粒可以透过滤纸.
解答 解:A、胶体不带电,胶粒带电,故电泳可以证明胶粒带电,故A错误;
B、分散质粒子直径在1-100nm之间的分散系为胶体,故B错误;
C、溶液、胶体和浊液的本质区别是分散质粒子直径大小,而不是丁达尔效应,故C错误;
D、胶粒可以透过滤纸,但不能透过半透膜,故D正确.
故选D.
点评 本题考查了分散系的分类、胶体的性质以及分散系之间的本质区别,应注意的是丁达尔效应是胶体所特有的性质,但不是本质特征.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
4.由CH2=CH2制备HO-CH2-CH2-OH,所发生的化学反应类型是( )
| A. | 加成反应、取代反应 | B. | 加成反应、消去反应 | ||
| C. | 氧化反应、加成反应 | D. | 消去反应、氧化反应 |
5.下列有关Na2CO3和NaHCO3性质的说法中,正确的是( )
| A. | 热稳定性:Na2CO3<NaHCO3 | |
| B. | 相同温度下,在水中的溶解度:Na2CO3<NaHCO3 | |
| C. | 等质量的Na2CO3和NaHCO3最多产生CO2的量:Na2CO3<NaHCO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3最多消耗盐酸的量:Na2CO3<NaHCO3 |
4.下列关于Na2CO3和NaHCO3性质的叙述中,不正确的是( )
| A. | 加入澄清石灰水都有白色沉淀生成 | |
| B. | 向NaOH溶液中通入过量的CO2可制得NaHCO3 | |
| C. | 向饱和Na2CO3溶液中通入足量的CO2没有明显现象 | |
| D. | 可利用稀盐酸来区别Na2CO3、NaHCO3两种无色溶液 |
1.现有a、b、c三个容器,a容器恒容恒温,b容器恒压恒温,c容器恒容绝热.在三个容器中各充入1mol I2(g)和2mol H2发生反应I2(g)+H2(g)?2HI(g)△H<0,初始时三个容器的体积和温度均相等,则反应达到平衡后,三个容器中I2(g)的转化率的大小关系是( )
| A. | a=b>c | B. | b>a>c | C. | c>b>a | D. | a=b<c |
2.常温下,下列离子在指定的溶液中一定能大量共存的是( )
| A. | [H+][OH-]=10-14mol2•L-2的溶液中:NH4+,Na+,SO42-,NO3- | |
| B. | pH=13的溶液中:Cu2+,K+,Cl-,NO3- | |
| C. | 滴入石蕊试液变红的溶液中:Ba2+,Na+,NO3-,HCO3- | |
| D. | NH4NO3溶液中:Na+,Al3+,Cl-,SO42- |
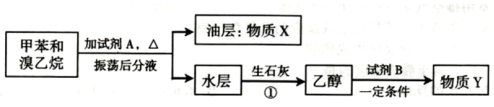
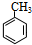 .
.