题目内容
10.把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是( )| A. | 溶液中Ca2+数目减少 | B. | 溶液pH值增大 | ||
| C. | 溶液中c(Ca2+)增大 | D. | 溶液pH值不变 |
分析 向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,消耗水,溶液c(Ca2+)、c(OH-)增大,由于原溶液已达到饱和,则平衡向逆反应方向移动,以此解答该题.
解答 解:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,加入CaO,消耗水,由于原溶液已达到饱和,则平衡向逆反应方向移动,溶液中Ca2+数目减少,反应后仍为饱和溶液,且满足温度不变,c(Ca2+)不变,c(OH-)不变,溶液pH不变,
故选AD.
点评 本题考查难溶电解质的溶解平衡,为高频考点,题目难度中等,本题注意向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,从平衡移动的角度分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.现有X、Y、Z、W四种金属片,①把X、Y用导线连接后同时浸入稀硫酸溶液中,X上有气泡产生,Y溶解;②把Z、W用导线连接后同时浸入稀硫酸溶液中,W发生还原反应;③把X、Z用导线连接后同时浸入稀硫酸溶液中,电子流动方向为X→导线→Z.根据上述情况判断正确的是( )
| A. | 在①中金属片Y发生还原反应 | |
| B. | 在②中金属片W作负极 | |
| C. | 上述四种金属的活动性顺序为W<X<Z<Y | |
| D. | 如果把Y、W用导线相连后同时浸入稀硫酸溶液,则电子流动方向为Y→导线→W |
6.下列事实不能作为实验判断依据的是( )
| A. | 钠和镁分别与冷水反应,判断金属活动性强弱:Na>Mg | |
| B. | 铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱:Cu>Na | |
| C. | 酸性H2CO3<H2SO4,判断硫与碳的非金属性强弱:S>C | |
| D. | F2与Cl2分别与H2反应,判断氟与氯的非金属性强弱:F>Cl |
3.表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | M与T形成的化合物既能与强酸反应又能与强碱反应 | |
| C. | L2+与R2-的核外电子数相等 | |
| D. | 单质分别与浓度相等的稀盐酸反应的速率为Q>L |
5.真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=1344.1kJ•mol-1
②2AlCl3(g)=2Al(s)+3Cl2(g)△H2=1169.2kJ•mol-1
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H3=Q kJ•mol-1
下列有关说法正确的是( )
①Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=1344.1kJ•mol-1
②2AlCl3(g)=2Al(s)+3Cl2(g)△H2=1169.2kJ•mol-1
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H3=Q kJ•mol-1
下列有关说法正确的是( )
| A. | 反应①中化学能转化为热能 | |
| B. | 反应②中若生成液态铝则反应热应大于△H2 | |
| C. | 反应③中1molAlCl3(g)生成时,需要吸收174.9kJ的热量 | |
| D. | 该生产工艺中能循环利用的物质只有AlCl3 |
2.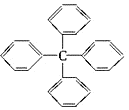 甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
 甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )| A. | 分子式为C25H20 | B. | 属于芳香烃 | ||
| C. | 该物质的一氯代物有3种 | D. | 所有碳原子可能都在同一平面上 |
19.标准状况下H2和Cl2组成的混合气体2.24L,经点燃充分反应后,缓缓通入100mL 1.2mol/LNaOH溶液中恰好完全反应,测得最终溶液中NaClO的浓度为0.2mol/L(假设溶液体积不变),则原混合气体中Cl2的体积分数(物质的量百分含量)为( )
| A. | 55% | B. | 60% | C. | 65% | D. | 70% |
20.如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )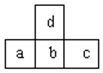

| A. | d的氢化物比b的氢化物稳定 | |
| B. | d与c不能形成化合物 | |
| C. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| D. | 原子半径的大小顺序是a>b>c>d |