��Ŀ����
5�����̼�Ȼ�ԭ-�Ȼ�����ʵ���������Ʊ�������������ص��Ȼ�ѧ����ʽ���£���Al2O3��s��+3C��s��=2Al��s��+3CO��g����H1=1344.1kJ•mol-1
��2AlCl3��g��=2Al��s��+3Cl2��g����H2=1169.2kJ•mol-1
��Al2O3��s��+3C��s��+3Cl2��g��=2AlCl3��g��+3CO��g����H3=Q kJ•mol-1
�����й�˵����ȷ���ǣ�������
| A�� | ��Ӧ���л�ѧ��ת��Ϊ���� | |
| B�� | ��Ӧ����������Һ̬����Ӧ��Ӧ���ڡ�H2 | |
| C�� | ��Ӧ����1molAlCl3��g������ʱ����Ҫ����174.9kJ������ | |
| D�� | ��������������ѭ�����õ�����ֻ��AlCl3 |
���� A����H1��0����Ϊ���ȷ�Ӧ���ʽ�����ת��Ϊ��ѧ�ܣ�
B��Al�ɹ�̬��ΪҺ̬���ȣ����Ը÷�Ӧ�������ӣ��䷴Ӧ�ȵ�ֵ���ڡ�H2��
C����֪��Al2O3��s��+3C��s��=2Al��s��+3CO��g����H1=1344.1kJ•mol-1
��2AlCl3��g��=2Al��s��+3Cl2��g����H2=1169.2kJ•mol-1
���ݸ�˹���ɣ���-�ڿɵã�Al2O3��s��+3C��s��+3Cl2��g��=2AlCl3��g��+3CO��g����
D����������������ѭ�����õ�����AlCl3��Cl2��
��� �⣺A����Ӧ�١�H1��0����Ϊ���ȷ�Ӧ���ʽ�����ת��Ϊ��ѧ�ܣ���A����
B��Al�ɹ�̬��ΪҺ̬���ȣ����Ը÷�Ӧ�������ӣ��䷴Ӧ�ȵ�ֵ���ڡ�H2����B��ȷ��
C����֪��Al2O3��s��+3C��s��=2Al��s��+3CO��g����H1=1344.1kJ•mol-1
��2AlCl3��g��=2Al��s��+3Cl2��g����H2=1169.2kJ•mol-1
���ݸ�˹���ɣ���-�ڿɵã�Al2O3��s��+3C��s��+3Cl2��g��=2AlCl3��g��+3CO��g����H3=174.9kJ•mol-1����1molAlCl3��g������ʱ����Ҫ����$\frac{1}{2}��174.9kJ$=87.45KJ����������C����
D����������������ѭ�����õ�����AlCl3��Cl2����D����
��ѡB��
���� ���⿼��������ת������Ӧ�ȵ��жϣ���Ӧ�ȵļ��㣬ѭ�����ʵ��жϣ������Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�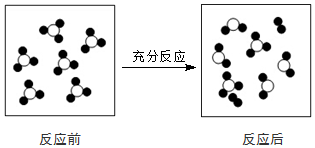
���ڴ˷�Ӧ˵��������ǣ�������
| A�� | һ�����ڷֽⷴӦ | B�� | һ������������ԭ��Ӧ | ||
| C�� | һ�����ڷ��ȷ�Ӧ | D�� | һ�����ڿ��淴Ӧ |
| A�� | ��ѧ����һ�������� | |
| B�� | ��ѧ������ʹԭ�����ϣ�Ҳ����ʹ�������� | |
| C�� | ��ѧ��Ӧ�����У���Ӧ������ڵĻ�ѧ�����ѣ���������ڵĻ�ѧ���γ� | |
| D�� | ���Լ�����һ�ֻ�ѧ�� |
| A�� | ����������Ⱦ����IJ���������β���ŷ��й� | |
| B�� | �����͵������մɶ������������ǽ������� | |
| C�� | ����̿�������������Ư�ף���Ư��ԭ����ͬ | |
| D�� | �����еij��������彡�������� |
| A�� | ��Һ��Ca2+��Ŀ���� | B�� | ��ҺpHֵ���� | ||
| C�� | ��Һ��c��Ca2+������ | D�� | ��ҺpHֵ���� |
2CO2��g��+6H2��g��?CH3OCH3��g��+3H2O��g����H
��֪����CO��g��+2H2��g��?CH3OH��g����H1=-90.7kJ•mol-1
��2CH3OH��g��?CH3OCH3��g��+H2O��g����H2=-23.5kJ•mol-1
��CO��g��+H2O��g��?CO2��g��+H2��g����H3=-41.2kJ•mol-1
��1����H=-122.5kJ•mol-1
��2��ij�¶��£�������̶�Ϊ2L���ܱ������н��з�Ӧ�٣���1mol CO��2mol H2��ϣ���ò�ͬʱ�̵ķ�Ӧǰ��ѹǿ��ϵ�����
| ʱ�䣨min�� | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ�ȣ�P��/Pǰ�� | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
��3����֪��ijѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�[n��H2��/n��CO2��]ʱ��CO2��ת������ͼ1��ʾ����ͼ�пɵó�������Ҫ���ɣ�
������Ͷ�ϱȣ�CO2��ת��������
�������¶ȣ�CO2��ת���ʽ��ͣ�
���¶�Խ�ͣ�����Ͷ�ϱ�ʹCO2��ת���������Խ������
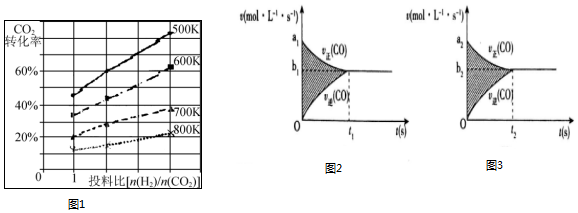
��4����Ӧ�۵�v-tͼ����ͼ2��ʾ���������������䣬ֻ���ڷ�Ӧǰ�����������ʹѹǿ��С������v-tͼ����ͼ3��ʾ��
����˵����ȷ����D
��a1��a2 ��a1��a2 ��b1��b2 ��b1��b2 ��t1��t2 ��t1=t2 ��t1��t2����ͼ����Ӱ���������� ����ͼ��Ӱ��������������ͼ��Ӱ�����������
A���٢ۢߢ�B���٢ۢݢ�C���ڢܢߢ�D���٢ۢߢ�
��5���ɼ״�Һ����ˮ��Ҳ���ƶ����ѣ����Ƚ��״���Ũ���ᷴӦ���������������CH3OSO3H����CH3OH+H2SO4��CH3OSO3H+H2O�����ɵ�����������ٺͼ״���Ӧ���ɶ����ѣ��ڶ����ķ�Ӧ����ʽΪ��CH3OSO3H+CH3OH��CH3OCH3+H2SO4����CO2��H2��Ӧ�Ʊ������ѱȽϣ��ù��յ��ŵ��Ƿ�Ӧ�¶ȵͣ�ת���ʸߣ���ȱ����ŨH2SO4��ʴ�豸���������Һ������
| A�� | C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g����H=-1 367.0 kJ•mol-1��ȼ���ȣ� | |
| B�� | NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=+57.3 kJ•mol-1���к��ȣ� | |
| C�� | S��s��+O2��g���TSO2��g����H=-296.8 kJ•mol-1����Ӧ�ȣ� | |
| D�� | C��s��+$\frac{1}{2}$O2��g���TCO��g����H=+110.5 kJ•mol-1��ȼ���ȣ� |
��1����Ӧ�����������仯��ͼ1��ʾ�������й�������ȷ����ac��
a���˷�ӦΪ���ȷ�Ӧ
b�������ܸı䷴Ӧ���ʱ�ͻ��
c��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ��
d���д����ܼӿ췴Ӧ���ʣ���߱����ת����
��2��������Ӧ�ں��º����ܱ������дﵽƽ�⣬��ƽ�ⳣ��K�ı���ʽΪK=$\frac{c��C{H}_{2}=C{H}_{2}��c��{H}_{2}��}{c��C{H}_{3}C{H}_{2}C{H}_{3}��}$�������£��÷�Ӧ��ƽ�ⳣ���������������С�����䡱��������������Ӧ�ﵽƽ�����������ͨ���������飬��$\frac{c��C{H}_{2}=CHC{H}_{3}��}{c��C{H}_{3}C{H}_{2}C{H}_{3}��}$��С�����������С�����䡱����
��3����0.1MPa��800K�����£�������ܱ�������ͨ������ϡ�����壬�������ⷴӦ��ת��������ϡ���������������ı仯�����ͼ2��ʾ��������ϡ�������������������ӣ�����ת�����������ԭ���Ǵ˷�Ӧ��������������ӵķ�Ӧ������ϡ��������������ӣ������˷�Ӧ��ϵ������ķ�ѹ���൱�ڼ�ѹ���Ӷ��ٽ���Ӧ������Ӧ������У�����˱��������ת���ʣ�

��4��������Ӧ�������ϩ���ಽ�������ɱ��ᣬ��֪������Ka��CH3CH2COOH��=1.3��10-5��Kb��NH3•H2O��=1.8��10-5��
�������ӷ���ʽ��ʾCH3CH2COONa��Һ�Լ��Ե�ԭ��CH3CH2COO-+H2O?CH3COOH+OH-��
�ڳ����£��������백ˮ��Ϻ���Һ�����ԣ�����Һ��$\frac{c��C{H}_{3}C{H}_{2}CO{O}^{-}��}{c��N{H}_{3}•{H}_{2}O��}$=1.3��109��
��5����֪��
| ��ѧ�� | H-H | C-H | C-C | C=C |
| ���ܣ�kJ•mol-1�� | 436 | 413 | 348 | 612 |
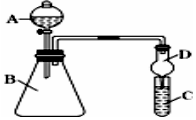 ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮