题目内容
12.如图所示的装置中,属于原电池的是( )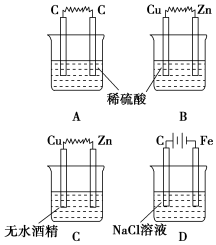
| A. | A | B. | B | C. | C | D. | D |
分析 原电池的构成条件为:①具有两个活性不同的电极;②有电解质溶液;③形成闭合回路;④对应常温下能自动发生的氧化还原反应(放热反应),以此来解答.
解答 解:A、两个电极相同,不能构成原电池,故A错误;
B、符合原电池的构成条件,属于原电池,故B正确;
C、酒精为非电解质,不能构成原电池,故C错误;
D、有外接电源,属于电解池,故D错误;
故选B.
点评 本题考查原电池的构成条件,明确图中金属的活泼性、电解质的判断、闭合回路的判断即可解答,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-.某同学设计并完成了如图的实验:下列说法正确的是( )


| A. | 溶液 A 中一定存在 NH4+、SO42-、SO32-,可能存在 Na+ | |
| B. | 溶液 A 中一定存在 NH4+、Mg2+、SO42-、SO32-,可能存在 Cl- | |
| C. | 溶液 A 中可能存在 Cl-,且 c(Na+)≥0.20 mol•L-1 | |
| D. | 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+ |
3.设NA为阿伏加德罗常数的值,下列说法中不正确的是( )
| A. | 1molC2H4Cl2中含有共用电子对数目为7NA | |
| B. | 标准状况下,44.8 L丙三醇与足量金属钠反应,生成气体的分子数为3NA | |
| C. | 20℃时,1 mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| D. | 15g甲基正离子(CH3+)所含有的电子数是8NA |
20.将CO2气体通入下列溶液中,无明显现象的是( )
| A. | NaAlO2溶液 | B. | Na2SiO3溶液 | C. | 漂白粉溶液 | D. | CaCl2 |
7.设NA为阿伏伽德罗常数值.下列有关叙述不正确的是( )
| A. | 5.8g熟石膏(2CaSO4•H2O)含有的结晶水分子数为0.02NA | |
| B. | 在K37ClO3+6H35Cl(浓)═KCl+3Cl2↑+3H2O反应中,若有212克氯气生成,则反应中电子转移的数目为5NA | |
| C. | 60克的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2 | |
| D. | 1mol CnH2n-2(n≥2)中所含的共用电子对数为(3n+1)NA |
17. 甲苯(
甲苯( 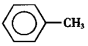 )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛( 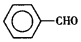 )、苯甲酸(
)、苯甲酸( 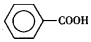 )等产品.表列出了有关物质的部分物理性质,请回答:
)等产品.表列出了有关物质的部分物理性质,请回答:
注:甲苯、苯甲醛、苯甲酸三者互溶.
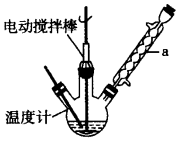
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)装置a的名称是冷凝管,主要作用是冷凝回流,防止甲苯的挥发而降低产品产率.
(2)三颈瓶中发生反应的化学方程式为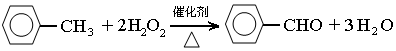
(3)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量.
(4)反应完毕后,反应混合液经过自然冷却至室温后,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸,若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合震荡.
 甲苯(
甲苯(  )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(  )、苯甲酸(
)、苯甲酸(  )等产品.表列出了有关物质的部分物理性质,请回答:
)等产品.表列出了有关物质的部分物理性质,请回答:| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度(ρ水=1g/cm3) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)装置a的名称是冷凝管,主要作用是冷凝回流,防止甲苯的挥发而降低产品产率.
(2)三颈瓶中发生反应的化学方程式为

(3)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量.
(4)反应完毕后,反应混合液经过自然冷却至室温后,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸,若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合震荡.
1.下列有机物的命名正确的是( )
| A. | 2,3,3-三甲基丁烷 | B. | 2-乙基-2-丁烯 | ||
| C. | 4-羟基苯甲酸 | D. | 二乙醇(HOOC-COOH) |
13.下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①NaHSO4②Al2O3 ③NaHSO3 ④(NH4)2CO3.
①NaHSO4②Al2O3 ③NaHSO3 ④(NH4)2CO3.
| A. | ②③④ | B. | ①②③④ | C. | ②③ | D. | ①②③ |



