题目内容
2.溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-.某同学设计并完成了如图的实验:下列说法正确的是( )
| A. | 溶液 A 中一定存在 NH4+、SO42-、SO32-,可能存在 Na+ | |
| B. | 溶液 A 中一定存在 NH4+、Mg2+、SO42-、SO32-,可能存在 Cl- | |
| C. | 溶液 A 中可能存在 Cl-,且 c(Na+)≥0.20 mol•L-1 | |
| D. | 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+ |
分析 溶液A加入过量氯化钡溶液生成沉淀B质量为4.50g沉淀,且沉淀部分溶解于稀盐酸,说明原来有SO32-,则原溶液中没有Mg2+、Ba2+,沉淀没有完全溶解,说明原溶液中有SO42-,且BaSO4的质量为2.33g,则说明原溶液中SO42-的物质的量为0.01mol,BaSO3的质量为4.50g-2.33g=2.17g,则SO32-的物质的量为0.01mol,溶液加入NaOH溶液生成448ml气体,为氨气,n(NH3)=$\frac{448ml}{22400ml}$=0.02mol,说明含有0.02molNH4+,则阴离子的电荷总数为2n(SO32-)+2n(SO42-)=2×0.01mol+2×0.01mol=0.04mol,则阳离子的电荷总数为n(NH4+)=0.02mol,0.04mol>0.02mol,根据电荷守恒溶液中肯定存在其它阳离子,故存在Na+,以此解答该题.
解答 解:溶液A加入过量氯化钡溶液生成沉淀B质量为4.50g沉淀,且沉淀部分溶解于稀盐酸,说明原来有SO32-,则原溶液中没有Mg2+、Ba2+,沉淀没有完全溶解,说明原溶液中有SO42-,且BaSO4的质量为2.33g,则说明原溶液中SO42-的物质的量为0.01mol,BaSO3的质量为4.50g-2.33g=2.17g,则SO32-的物质的量为0.01mol,溶液加入NaOH溶液生成448ml气体,为氨气,n(NH3)=$\frac{448ml}{22400ml}$=0.02mol,说明含有0.02molNH4+,则阴离子的电荷总数为2n(SO32-)+2n(SO42-)=2×0.01mol+2×0.01mol=0.04mol,则阳离子的电荷总数为n(NH4+)=0.02mol,0.04mol>0.02mol,根据电荷守恒溶液中肯定存在其它阳离子,故存在Na+,
A.根据上述分析溶液 A 中一定存在NH4+、SO42-、SO32-、Na+,故A错误;
B.根据上述分析溶液 A 中一定存在NH4+、SO42-、SO32-、Na+,可能存在 Cl-,故B错误;
C.溶液 A 中可能存在 Cl-,则阴离子的电荷总数为2n(SO32-)+2n(SO42-)+n(Cl-)=2×0.01mol+2×0.01mol=0.04mol+n(Cl-),阳离子的电荷总数为n(NH4+)+n(Na+)=0.02mol+n(Na+),根据电荷守恒,则0.04mol+n(Cl-)=0.02mol+n(Na+),则n(Na+)=0.02mol+n(Cl-),故n(Na+)≥0.02mol,故c(Na+)≥0.20 mol•L-1,故C正确;
D.NH4+检验用湿润的红色石蕊试纸变蓝,说明溶液中一定含有NH4+,故D错误,
故选C.
点评 本题考查无机物的推断,为高频考点,把握实验中发生的反应、现象与结论的关系为解答的关键,侧重分析与实验能力的考查,题目难度不大.

| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 溶液温度降低主要是因为NH4HCO3溶解吸热造成的 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 反应的热化学方程式为:NH4HCO3+HCl→NH4Cl+CO2↑+H2O-Q |
| A. | 常温下,苯酚易溶于水 | |
| B. | 苯酚俗称石炭酸,具有微弱的酸性,能与碳酸钠溶液反应 | |
| C. | 能与FeCl3溶液作用显紫色的有机物一般含有酚羟基 | |
| D. | 洒落皮肤上的苯酚可以用氢氧化钠稀溶液洗涤 |
| 实验步骤 | 有关问题 |
| (1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为10.6g. |
| (2)称量Na2CO3固体 | 称量过程中主要用到的仪器是托盘天平、砝码、药匙. |
| (3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是用玻棒搅拌或加热 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是用玻璃棒引流 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是当加水璃刻度线1-2cm时改用胶头璃管加水至凹液面与刻度线相切 |
| A. | 具有相同电子层数而又按原子序数递增顺序排列的横行称为周期 | |
| B. | 元素周期表共有14列元素:7个主族和7个副族 | |
| C. | 元素周期表的第一列元素称为第IA族,均为活泼的金属元素 | |
| D. | 元素周期表中第二周期第VIIA族元素的最高正价为+7价 |
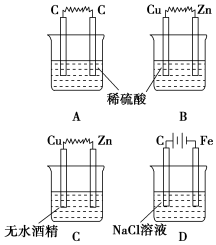
| A. | A | B. | B | C. | C | D. | D |
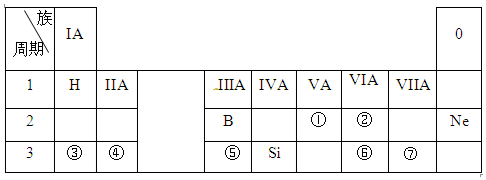
 ;
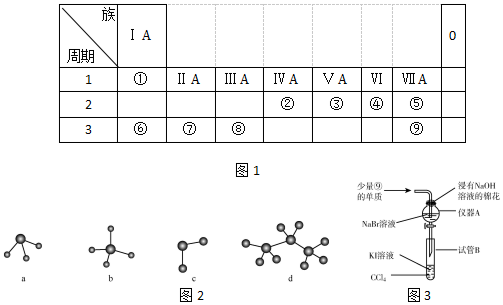
;
 .
. →
→ ,元素⑥和⑨形成的化合物中含有离子键.
,元素⑥和⑨形成的化合物中含有离子键.