题目内容
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | lmo1CH4中含有的电子数为9NA | |
| B. | 0.1mol•L-1的Na2S溶液中所含阴离子的数目大于0.1NA | |
| C. | 1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为2NA | |
| D. | 80℃时,1LNaCl溶液中含有OH-的数目为1×10-7NA |
分析 A.1个甲烷分子含有10个电子;
B.溶于体积未知;
C.镁与氧气或者氮气反应均生成二价镁离子;
D.80℃时,Kw未知,无法计算氯化钠溶液中氢氧根离子浓度;
解答 解:A.lmo1CH4中含有的电子数为10NA,故A错误;
B.依据n=CV可知,溶液体积未知无法计算微粒个数,故B错误;
C.MgO和Mg3N2的混合物中镁的化合价都为+2价,1mol镁变成镁离子生成2mol电子,共失去2NA个电子,故C正确;
D.80℃时,Kw未知,无法计算氯化钠溶液中氢氧根离子浓度,无法计算氢氧根离子数目,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算及应用,明确以物质的量为核心计算公式是解题关键,注意Kw与温度有关,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
3.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol硫单质在过量氧气中燃烧产生NA个SO3分子 | |
| B. | 标准状况下,22.4LSO3中含有氧原子数为3NA | |
| C. | 标准状况下,18gH2O中含有氧原子数为NA | |
| D. | 5.4g铝单质与足量NaOH溶液反应,转移电子数为0.6NA |
4.如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
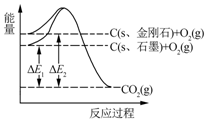

| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ热量 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol金刚石和1 mol O2化学键断裂吸收的能量总和大于1 mol CO2分子中化学键断裂吸收的能量 |
1.北学与生活密切相关,下列叙述中不正确的是( )
| A. | 糖类是人体能量的主要来源 | |
| B. | 食盐可作调味剂,也可作食品防腐剂 | |
| C. | 天然存在的动植物油脂,大多属于单甘油酯 | |
| D. | 乙烯可作水果催熟剂,能促进水果尽早成熟 |
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11g CO2含有的共用电子对数为0.5NA | |
| B. | 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA | |
| C. | 通常状况下,39 g Na2O2固体中含有的离子总数为2NA | |
| D. | 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA |
18.化学在工农业生产和日常生活中都有重要应用.下列叙述正确的是( )
| A. | 油脂和蛋白质是人体必需的营养物质,都属于高分子化合物 | |
| B. | 食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是防止食品氧化变质 | |
| C. | 城际“轻轨电车”启动时,电车电刷与导线的接触点会产生高温,石墨可用作接触点上的材料 | |
| D. | 中医古籍《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”启发了屠呦呦,采用低温提取,解决了关键性的技术难题.青蒿素的提取属于化学变化 |
5.下列有关乙二酸(HOOC-COOH)的说法中正确的是(设NA为阿伏加德罗常数的值)( )
| A. | 标准状况下90g乙二酸所占的体积约为22.4L | |
| B. | lmol乙二酸中含有共用电子对的数目为9NA | |
| C. | 90g乙二酸被NaC1O氧化生成CO2,转移的电子数为NA | |
| D. | 0.lmol•L-1的乙二酸溶液中,H2C2O4、C2O2-和HC2O4-的微粒数之和为0.1NA |
2.对未知溶液,下列实验事实陈述正确,并且Ⅰ和Ⅱ有因果关系的是( )
| Ⅰ操作 | Ⅱ结论 | |
| A | 滴加BaC12溶液生成白色沉淀 | 原溶液中有SO42- |
| B | 用洁净铂丝蘸取溶液进行焰色反应:火焰呈黄色 | 原溶液中有Na+无K+ |
| C | 滴加氯水和CC14,振荡、静置.下层溶液显紫色 | 原溶液中一定有KI |
| D | 向盐溶液中滴加几滴浓NaOH溶液,微热,再将湿润红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
14.证明某溶液含有Fe2+的实验方法是( )
| A. | 先滴加氯水,再滴加KSCN溶液后显红色 | |
| B. | 先滴加KSCN溶液,不显红色,再滴加氯水后显红色 | |
| C. | 滴加NaOH溶液,产生白色沉淀 | |
| D. | 只需滴加KSCN溶液 |