题目内容
25℃时,下列溶液中微粒存在情况合理的是( )
| A、Fe2+、Mg2+、ClO-、Cl-能大量共存 | ||
| B、滴入酚酞试液显红色的溶液中:K+、Na+、NO3-、SO42- | ||
C、含大量K+、Na+、NO3-、CO32-的溶液中c(H+)=
| ||
| D、C(Fe3+)=0.1 mol/L的溶液中:NH4+、Al3+、I-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.Fe2+与ClO-发生氧化还原反应;
B.离子之间不发生任何反应,且与SO2不反应;
C.c(H+)=
,说明溶液中c(H+)=c(OH-),溶液呈中性;
D.铁离子具有氧化性能氧化I-.
B.离子之间不发生任何反应,且与SO2不反应;
C.c(H+)=
| Kw |
D.铁离子具有氧化性能氧化I-.
解答:
解:A.Fe2+具有还原性,ClO-具有强氧化性,二者可发生氧化还原反应而不能大量共存,故A错误;
B.滴入酚酞试液显红色的溶液显碱性:K+、Na+、NO3-、SO42-,可大量共存,故B正确;
C.c(H+)=
,说明溶液中c(H+)=c(OH-),溶液呈中性,而CO32-水解呈碱性,故C错误;
D.铁离子具有氧化性能氧化I-,2Fe3++2I-=2Fe2++I2,不能大量共存,故D错误.
故选B.
B.滴入酚酞试液显红色的溶液显碱性:K+、Na+、NO3-、SO42-,可大量共存,故B正确;
C.c(H+)=
| Kw |
D.铁离子具有氧化性能氧化I-,2Fe3++2I-=2Fe2++I2,不能大量共存,故D错误.
故选B.
点评:本题综合考查离子共存问题,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握离子的性质和反应类型的判断,答题时注意审题,难度不大.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
常温下,下列各组离子一定能大量共存的是( )
| A、滴加石蕊显红色的溶液中:Na+、Fe2+、Cl-、NO3- | ||
B、
| ||
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- | ||
| D、由水电离的c(H+)=1.0×10-13 mol?L-1的溶液中:K+、NH4+、AlO2-、HCO3- |
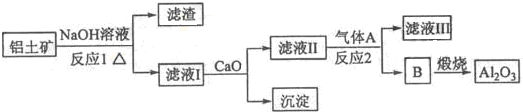
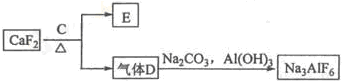
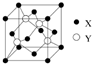 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.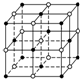 地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素.它们在化学中占有极其重要的地位.
地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素.它们在化学中占有极其重要的地位.