题目内容
4.下列物质分类正确的是( )| A. | SO2、SiO2、CO均为酸性氧化物 | B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | ||
| C. | 盐酸、水玻璃、氨水均为混合物 | D. | 烧碱、冰醋酸、四氯化碳均为电解质 |
分析 A.酸性氧化物是指和碱反应生成盐和水的氧化物,发生的是复分解反应;
B.分散质微粒直径在1-100nm的形成的分散系为胶体;
C.不同物质组成的为混合物;
D.水溶液中或熔融状态下导电的化合物为电解质.
解答 解;A.SO2、SiO2和碱反应生成盐和水均为酸性氧化物,CO和碱不反应属于不成盐氧化物,故A错误;
B.稀豆浆、硅酸均为胶体,氯化铁溶液不是胶体,故B错误;
C.盐酸是氯化氢水溶液、水玻璃是硅酸钠水溶液、氨水是氨气的水溶液均为混合物,故C正确;
D.烧碱是氢氧化钠、冰醋酸水溶液导电,所以均为电解质,四氯化碳水溶液中不能导电属于非电解质,故D错误;
故选C.
点评 本题考查了物质分类、物质组成、物质名称、掌握概念实质是解题关键,题目难度不大.

练习册系列答案
相关题目
14.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C16H22O5 | B. | C14H16O4 | C. | C14H18O5 | D. | C14H20O5 |
15.元素周期表中 VIA族2~5周期元素分别为氧(O)、硫(S)、硒(Se)、碲(Te),它们的单质与H2反应生成1mol气态氢化物的反应热如下.其中表示生成1mol硒化氢(H2Se)反应热的是( )
| A. | +99.7kJ•mol-1 | B. | +29.7kJ•mol-1 | C. | -20.6kJ•mol-1 | D. | -241.8kJ•mol-1 |
12.下列叙述不正确的是( )
| A. | 常温常压下,3.2g O 2所含的原子数为0.2NA | |
| B. | 标准状况下,18g H2 O所含的氧原子数目为NA | |
| C. | 常温常压下,92g NO2和N2O 4的混合气体中含有的原子总数为6 NA | |
| D. | 标准状况下,22.4LCH4与22.4L N2所含原子数均为2 NA |
9.亚硫酸盐是一种常见的食品添加剂,用如图实验可检验某食品中亚硫酸盐含量(所 加试剂均足量).
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 亚硫酸盐作为食品添加剂,作用是防腐保鲜 | |
| B. | 反应①过程中通入N2的作用是将装置中空气和生成的气体全部赶出 | |
| C. | 测定样品质量及③中耗碱量,可测定样品中亚硫酸盐含量 | |
| D. | 若仅将②中的氧化剂“H2O2溶液”替换为碘水,对测定结果无影响 |
 .
.

 .
.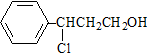 $→_{△}^{O_{2}/Cu}$$→_{Ⅱ}^{一定条件}$乙
$→_{△}^{O_{2}/Cu}$$→_{Ⅱ}^{一定条件}$乙 ,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.
,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化. 为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”,其主题为“化学──我们的生活,我们的未来”.化学关注食品安全、人类健康和社会的可持续发展,为改善人类生活质量、提高人类生活水平发挥了重要作用.请回答下列问题:
为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”,其主题为“化学──我们的生活,我们的未来”.化学关注食品安全、人类健康和社会的可持续发展,为改善人类生活质量、提高人类生活水平发挥了重要作用.请回答下列问题: