题目内容
11.草酸合铁酸钾晶体Kx[Fe(C2O4)y]•3H2O是一种光敏材料,见光易分解,下面是一种制备草酸合铁酸钾晶体的实验流程.
已知:(NH4)2SO4、FeSO4•7H2O、莫尔盐[(NH4)2SO4•FeSO4•6H2O]的溶解度如表:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4•7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | - |
| (NH4)2SO4•FeSO4•6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(2)“溶解1”应保证铁屑稍过量,其目的是防止Fe2+被氧化为Fe3+.“溶解2”加“几滴H2SO4”的作用是防止Fe2+水解.
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、冷却结晶、过滤、用乙醇洗涤、干燥.用乙醇洗涤的目的是冷却结晶,洗去杂质,减少莫尔盐晶体溶解损失,便于快速干燥.
(4)“沉淀2”时得到的FeC2O4•2H2O沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是
用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净
(5)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是黑暗可以防止晶体分解.
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤
【备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液】:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250mL待测液.
步骤2:用移液管移取25.00mL待测液于锥形瓶中,加入稀H2SO4酸化,加入足量KMnO4溶液,使C2O42-转化为CO2被除去.
步骤3:向步骤2所得溶液中加入稍过量的锌粉,加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中
步骤4:用c mol•L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液.
分析 废铁屑加入硫酸溶液溶解,加入硫酸铵溶液结晶析出硫酸亚铁晶体,加水溶解,滴入几滴稀硫酸防止亚铁离子水解,加入草酸沉淀亚铁离子,过滤得到沉淀加入重铬酸钾、过氧化氢溶液氧化加入草酸得到草酸合铁酸钾晶体;
(1)在5% Na2CO3溶液中加热数分钟,并洗涤干净是利用碳酸钠水解显碱性,去除油污;
(2)铁过量防止亚铁离子被氧化,滴入稀硫酸防止硫酸亚铁水解;
(3)复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩,冷却结晶,过滤用乙醇洗涤、干燥,防止生成的盐损失,乙醇易挥发;
(4)取最后一次洗涤液,检查是否含有硫酸根离子进行设计分析;
(5)晶体易分解;
(6)步骤1:称量ag三草酸合铁酸钾晶体,配制成250mL溶液;
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+;
步骤3:向反应后的溶液中加入适量锌粉使Fe3+全部转化为Fe2+,同时有气泡产生,过滤,洗涤,将过滤及洗涤所得溶液A收集到锥形瓶中,此时,溶液仍呈酸性;
步骤4:用cmol/L KMnO4溶液滴定溶液至终点,消耗KMnO4溶液Vml,反应中MnO4-被还原成Mn2+.
解答 解:废铁屑加入硫酸溶液溶解,加入硫酸铵溶液结晶析出硫酸亚铁晶体,加水溶解,滴入几滴稀硫酸防止亚铁离子水解,加入草酸沉淀亚铁离子,过滤得到沉淀加入重铬酸钾、过氧化氢溶液氧化加入草酸得到草酸合铁酸钾晶体;
(1)在5% Na2CO3溶液中加热数分钟,并洗涤干净是利用碳酸钠水解显碱性,油污会发生水解生成溶于水的物质洗去,作用是去除油污;
故答案为:除油污;
(2)铁过量防止亚铁离子被氧化,“溶解1”应保证铁屑稍过量,其目的是防止Fe2+被氧化为Fe3+;滴入稀硫酸防止硫酸亚铁水解,.“溶解2”加“几滴H2SO4”的作用抑制Fe2+水解;
故答案为:防止Fe2+被氧化为Fe3+;抑制Fe2+水解;
(3)复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩,冷却结晶,过滤用乙醇洗涤、干燥,防止生成的盐损失,乙醇易挥发;
故答案为:冷却结晶,洗去杂质,减少莫尔盐晶体溶解损失,便于快速干燥;
(4)取最后一次洗涤液,检查是否含有硫酸根离子进行设计分析,用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净;
故答案为:用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净;
(5)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是黑暗可以防止晶体分解;
故答案为:黑暗可以防止晶体分解;
(6)步骤1:称量ag三草酸合铁酸钾晶体,配制成250mL溶液;
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+;
步骤3:向反应后的溶液中加入适量锌粉使Fe3+全部转化为Fe2+,同时有气泡产生,过滤,洗涤,将过滤及洗涤所得溶液A收集到锥形瓶中,此时,溶液仍呈酸性;
步骤4:用cmol/L KMnO4溶液滴定溶液至终点,消耗KMnO4溶液Vml,反应中MnO4-被还原成Mn2+;
故答案为:加入足量KMnO4溶液;加入稍过量的锌粉,加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中.
点评 本题考查了物质制备流程,为高频考点,涉及实验基本操作、盐类水解、氧化还原反应等知识点,明确流程图中发生的反应及溶液中存在微粒是解本题关键,熟练掌握离子检验、基本操作、反应原理等,题目难度中等.

| A. | 酒精、汽油都是有机溶剂,可以清洗衣服上的油污斑点 | |
| B. | 硫酸可以作铅蓄电池的电解质,也可用于溶解除去锅炉和水壶里的水垢 | |
| C. | 废旧塑料制品、废旧金属制品要回收和利用 | |
| D. | 推广太阳能、风能等新能源技术是施行低碳经济的有效途径 |
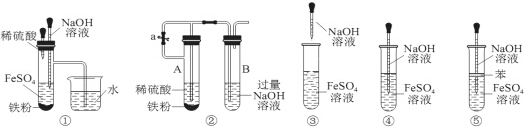
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ①②③④ | D. | ②④⑤ |
| A. | 已知:①2H2(g)+O2(g)═2H2O(g)△H1=-a kJ•mol-1, ②2H2(g)+O2(g)═2H2O(l)△H2=-b kJ•mol-1, 则a>b,△H1<△H2 | |
| B. | 同温同压下,SO2(g)+2CO(g)═2CO2(g)+S(l)在有无催化剂条件下的△H不同 | |
| C. | 任何酸与碱发生中和反应生成1mol H2O的过程中,能量变化均相同 | |
| D. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含2.0 g氢氧化钠的稀溶液与稀盐酸完全中和,放出热量2.865 kJ |
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是吸热(填“吸热”或“放热”)反应.
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有CE(填写字母序号).
A、缩小反应容器的容积 B、扩大反应容器的容积 C、升高温度
D、使用合适的催化剂 E、设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:
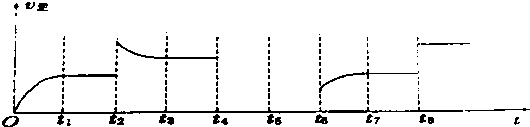
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物浓度或升高温度,t8时加入催化剂或加压.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
| A. | Ca2(OH)(PO4)3 | B. | Ca3(OH)(PO4)3 | C. | Ca4(OH)(PO4)3 | D. | Ca5(OH)(PO4)3 |
| A. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |