题目内容
7.如表实验操作、现象与结论对应关系正确的是( )| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有Fe(NO3)2溶液的试管中加入0.1mol•L-1 H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体, | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
| A. | A | B. | B | C. | C | D. | D |
分析 A.酸性条件下NO3-被Fe2+还原为NO;
B.含有酚酞的Na2CO3溶液,因碳酸根离子水解显碱性溶液变红,加入少量BaC12固体,水解平衡逆向移动,则溶液颜色变浅;
C.HX放出的氢气多且反应速率快,说明HX浓度比HY大;
D.亚硫酸不是最高价含氧酸,则不能比较非金属性.
解答 解:A.酸性条件下NO3-被Fe2+还原为NO,NO能被氧气氧化为NO2,故A错误;
B.含有酚酞的Na2CO3溶液,因碳酸根离子水解显碱性溶液变红,加入少量BaC12固体,水解平衡逆向移动,则溶液颜色变浅,证明Na2CO3溶液中存在水解平衡,故B正确;
C.HX放出的氢气多且反应速率快,说明HX浓度比HY大,HX酸性比HY弱,故C错误;
D.等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大,可比较亚硫酸与碳酸的酸性,因亚硫酸不是最高价含氧酸,则不能比较非金属性,故D错误.
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化还原反应、盐类的水解、酸性比较以及非金属比较等,把握反应原理及反应与现象的关系为解答的关键,注意从实验的评价性及物质性质分析解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀.
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(保准状况).
下列说法正确的是( )
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀.
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(保准状况).
下列说法正确的是( )
| A. | 该固体中一定含有NH4+、CO32-、SO42-、Na+ | |
| B. | 该固体中一定没有Cu2+、Cl-、Na+ | |
| C. | 该固体中只含有NH4+、CO32-、SO42-、Cl- | |
| D. | 根据以上实验,无法确定该固体中有Na+ |
18.X、Y、Z、W是原子序数依次增大的四种短周期元素.Y和Z位于同一周期,可组成中学常见的共价化合物YZ和YZZ,X和Z的原子最外层电子数之和等于W的原子最外层电子数,25℃时0.01mol/L X和W形成化合物的水溶液pH为2.下列说法正确的是( )
| A. | Y元素含氧酸的酸性比W的弱 | |
| B. | Z和W在自然界均能以游离态存在 | |
| C. | YZ和YZ2均可以被NaOH溶液吸收 | |
| D. | X和Y能形成既含极性键又含非极性键的分子 |
15.分子式为C4H8O2且能与氢氧化钠溶液反应的有机物(不考虑立体异构和醛类物质)有( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
2.化学与生产、生活、社会密切相关.下列说法中正确的是( )
| A. | 漂白粉长期放置会被空气中的氧气氧化而变质 | |
| B. | 不锈钢具有较强的耐腐蚀性,纯铁也有较强的耐腐蚀性 | |
| C. | 汽车尾气中氮氧化物的产生主要是由于汽油中含有氮元素而产生的 | |
| D. | 对石油进行分馏可以得到许多苯的同系物 |
19.下列实验操作对应的现象和结论均正确的是( )
| 序号 | 操作 | 现象 | 结论 |
| A | 在盛番茄汤的玻璃杯中加入适量植物油,充分搅拌、静置 | 上层溶液颜色比下层更深 | 番茄色素在植物油中的溶解度比在水中小 |
| B | 向浓度均为0.1mol/L的醋酸和硼酸的溶液中分别滴加等浓度Na2CO3溶液 | 前者产生大量气泡,后者无现象 | 酸性强弱顺序:醋酸>碳酸>硼酸 |
| C | 将碳酸氢铵分解产生的气体通入CaC12溶液 | 产生白色沉淀 | CO2与CaC12溶液反应生成CaCO3沉淀 |
| D | 在试管中将某有机物与银氨溶液混合微热 | 产生光亮的银镜 | 该有机物一定是醛类物质 |
| A. | A | B. | B | C. | C | D. | D |
16.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 6.0gSiO2晶体中存在的共价键总数为2 NA | |
| B. | 1L 0.1mol•L-1的Na2CO3溶液中含有阳离子的总数为2NA | |
| C. | 标准状况下,2.0gD2O中含有的质子数和中子数均为NA个 | |
| D. | 室温时,pH=12的Ba(OH)2溶液中,氢氧根离子数目为10-2N |
17.如表实验操作可以达到目的是( )
| 目的 | 操作 | |
| A | 干燥Cl2 | 将气体通过盛有碱石灰的干燥装置 |
| B | 检验溴乙烷中的溴元素 | 取样,加NaOH溶液,振荡后再加AgNO3溶液 |
| C | 测定混有NaCl的Na2CO3固体样品中Na2CO3的质量分数 | 取m1g样品加入过量盐酸充分反应,加热蒸干后,称量固体质量为m2 g |
| D | 配制100mL 1.0mol•L-1 CuSO4溶液 | 将25g CuSO4•5H2O溶于100mL蒸馏水中 |
| A. | A | B. | B | C. | C | D. | D |

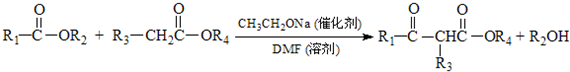
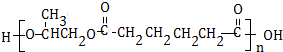 .
.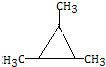 .
.