题目内容
将Na2CO3?10H2O和NaHCO3的混合物11.94g,溶于水配制成200mL溶液,测得溶液中Na+浓度为0.5mol/L.若将11.94g该混合物加热至质量不再改变时,得到的固体物质的质量为( )
| A、1.06 g |
| B、3.1 g |
| C、5.3 g |
| D、9.0 g |
考点:有关混合物反应的计算
专题:计算题
分析:Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
n(Na+),根据n=cV计算混合物中含有的n(Na+),再根据m=nM计算最终得到的固体碳酸钠的质量.
| 1 |
| 2 |
解答:
解:混合物中含有的n(Na+)=cv=0.2L×0.5mol/L=0.1mol,
Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
n(Na+)=0.1mol×
=0.05mol,最终得到的固体碳酸钠的质量为0.05mol×106g/mol=5.3g,
故选C.
Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
| 1 |
| 2 |
| 1 |
| 2 |
故选C.
点评:本题考查混合物的有关计算,题目难度中等,注意利用钠离子守恒进行的计算,侧重对学生思维能力的考查.

练习册系列答案
相关题目
已知某反应的过程可用球棍模型表示如图:

下列说法不正确的是( )

下列说法不正确的是( )
| A、该过程表示的反应为:2H2+O2═2H20 |
| B、过程Ⅰ是吸热过程,过程Ⅲ是放热过程 |
| C、过程Ⅱ有化学键断裂 |
| D、该反应的能量变化不一定是热能形式 |
下列说法正确的是( )
①可用Ba(OH)2溶液同时鉴别AgNO3、AlCl3、NH4Cl、NaCl、Na2SO4五种溶液
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>H2SO4,所以非金属性:Cl>S
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤.
①可用Ba(OH)2溶液同时鉴别AgNO3、AlCl3、NH4Cl、NaCl、Na2SO4五种溶液
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>H2SO4,所以非金属性:Cl>S
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤.
| A、①②⑤ | B、①②④ |
| C、②④⑤ | D、全部 |
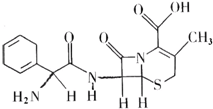 头孢拉定片(Cefradine Tablets),又称先锋霉素,该药品适宜敏感菌所导致的急性咽炎,扁桃体炎,中耳炎等呼吸道感染.其结构式如图所示,有关该物质的描述不正确的是( )
头孢拉定片(Cefradine Tablets),又称先锋霉素,该药品适宜敏感菌所导致的急性咽炎,扁桃体炎,中耳炎等呼吸道感染.其结构式如图所示,有关该物质的描述不正确的是( )| A、分子式为C16H20N3O4S |
| B、该物质在一定条件下能发生水解 |
| C、该有机物质不属于芳香族化合物 |
| D、该物质能与NaHCO3溶液反应放出CO2 |
把含有氧化铁的铁投入到足量的稀硫酸中,直到固体全部溶解,经分析,溶液中无Fe3+,且生成Fe2+与反应产生氢气的物质的量之比为8:5,原混合物中单质铁的质量分数为( )
| A、26.3% | B、73.7% |
| C、67.7% | D、95% |
下列高分子材料所含成分相同的是( )①棉纤维 ②人造棉 ③人造丝 ④蚕丝 ⑤合成羊毛.
| A、①②③ | B、②③④ |
| C、④⑤ | D、全部 |


