题目内容
下列说法正确的是( )
①可用Ba(OH)2溶液同时鉴别AgNO3、AlCl3、NH4Cl、NaCl、Na2SO4五种溶液
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>H2SO4,所以非金属性:Cl>S
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤.
①可用Ba(OH)2溶液同时鉴别AgNO3、AlCl3、NH4Cl、NaCl、Na2SO4五种溶液
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>H2SO4,所以非金属性:Cl>S
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤.
| A、①②⑤ | B、①②④ |
| C、②④⑤ | D、全部 |
考点:物质的检验和鉴别的基本方法选择及应用,分散系、胶体与溶液的概念及关系,电解质与非电解质,物质的分离、提纯和除杂
专题:
分析:①Ba(OH)2溶液与AgNO3、AlCl3、NH4Cl、Na2SO4现象不同;
②蔗糖为非电解质,水和硫酸钡都为电解质,但水为极弱电解质;
③比较非金属性的角度错误;
④胶体的本质特征是粒子直径介于1~100nm之间;
⑤铝可与氢氧化钠溶液反应.
②蔗糖为非电解质,水和硫酸钡都为电解质,但水为极弱电解质;
③比较非金属性的角度错误;
④胶体的本质特征是粒子直径介于1~100nm之间;
⑤铝可与氢氧化钠溶液反应.
解答:
解:①加入Ba(OH)2溶液,AgNO3生成灰色沉淀氧化银,AlCl3先生成沉淀,后溶解,NH4Cl生成刺激性气体,NaCl不反应,无现象,Na2SO4生成白色沉淀,现象不同,可鉴别,故正确;
②蔗糖为非电解质,水和硫酸钡都为电解质,但水为极弱电解质,硫酸钡为强电解质,故正确;
③应从最高价氧化物的水化物的酸性的角度比较非金属性强弱,故错误;
④胶体的本质特征是粒子直径介于1~100nm之间,故错误;
⑤铝可与氢氧化钠溶液反应,可用于除杂,故正确.
故选A.
②蔗糖为非电解质,水和硫酸钡都为电解质,但水为极弱电解质,硫酸钡为强电解质,故正确;
③应从最高价氧化物的水化物的酸性的角度比较非金属性强弱,故错误;
④胶体的本质特征是粒子直径介于1~100nm之间,故错误;
⑤铝可与氢氧化钠溶液反应,可用于除杂,故正确.
故选A.
点评:本题考查较为综合,设计物质的检验、分离以及胶体等知识,为高考常见题型,侧重于学生的双基的考查,注意相关知识的积累,难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
为了检验某卤代烃(R-X)中的X元素,在下列实验操作中:①加热②加入硝酸银溶液③取少量卤代烃④加入稀硝酸溶液酸化⑤加入氢氧化钠溶液⑥冷却,所选择的正确的操作顺序是( )
| A、③⑤④② |
| B、③⑤①④② |
| C、③⑤①⑥② |
| D、③⑤①⑥④② |
将Na2CO3?10H2O和NaHCO3的混合物11.94g,溶于水配制成200mL溶液,测得溶液中Na+浓度为0.5mol/L.若将11.94g该混合物加热至质量不再改变时,得到的固体物质的质量为( )
| A、1.06 g |
| B、3.1 g |
| C、5.3 g |
| D、9.0 g |


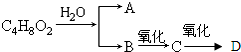
 A、B、C、D均为含有苯环的有机物,且式量B>A>C.己知有机物A既能和氢氧化钠溶液反应,又能和 NaHCO3溶液反应,并已知A的化学式为C7H6O3,且它的苯环上一氯代物有两种.
A、B、C、D均为含有苯环的有机物,且式量B>A>C.己知有机物A既能和氢氧化钠溶液反应,又能和 NaHCO3溶液反应,并已知A的化学式为C7H6O3,且它的苯环上一氯代物有两种.