题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、1L 0.1mol/L的Na2CO3溶液中,含Na+0.2 NA个,CO32-0.1 NA个 |
| B、1L 0.3mol/L的K2SO4溶液中,含K+和SO42-离子总数为0.9 NA个 |
| C、2L 0.6mol/L的Fe2(SO4)3溶液中,含SO42-离子总数为2.4 NA个 |
| D、0.1mol/L的H3PO4溶液中,c(H+):c(PO43-)<3:1 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、CO32-是弱酸根,在水溶液中会水解;
B、根据n=cV计算硫酸钾的物质的量,1molK2SO4含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
C、根据n=cV计算硫酸铁的物质的量,1molFe2(SO4)3含有3molSO42-;
D、H3PO4是中强酸,不能完全电离.
B、根据n=cV计算硫酸钾的物质的量,1molK2SO4含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
C、根据n=cV计算硫酸铁的物质的量,1molFe2(SO4)3含有3molSO42-;
D、H3PO4是中强酸,不能完全电离.
解答:
解:A、CO32-是弱酸根,在水溶液中会水解,故CO32-个数小于0.1 NA个,故A错误;
B、1L 0.3mol/LK2SO4溶液中所含K+、SO42-总数为1L×0.3mol/L×3×NA=0.9NA,故B正确;
C、2L 0.6mol/L的Fe2(SO4)3溶液中硫酸铁的物质的量n=CV=1.2mol,故含SO42-离子的物质的量为3.6mol,总数为3.6 NA个,故C错误;
D、H3PO4是中强酸,不能完全电离,故c(H+):c(PO43-)>3:1,故D错误.
故选B.
B、1L 0.3mol/LK2SO4溶液中所含K+、SO42-总数为1L×0.3mol/L×3×NA=0.9NA,故B正确;
C、2L 0.6mol/L的Fe2(SO4)3溶液中硫酸铁的物质的量n=CV=1.2mol,故含SO42-离子的物质的量为3.6mol,总数为3.6 NA个,故C错误;
D、H3PO4是中强酸,不能完全电离,故c(H+):c(PO43-)>3:1,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列说法错误的是( )
| A、由电能转化为化学能的装置叫电解池 |
| B、在电解池中跟直流电源的正极相连的电极是电解池的阳极 |
| C、在电解池中通电时,电子从电解池的阴极流出,并沿导线流回电源的负极 |
| D、电解池中阴极发生还原反应,阳极发生氧化反应 |
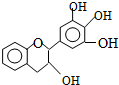 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A、分子中只有2个手性碳原子 |
| B、1molEGC与4molNaOH恰好完全反应 |
| C、可发生氧化反应和取代反应,不能发生加成反应 |
| D、遇FeCl3溶液会发生显色反应 |
同温同压下,下列各组热化学方程式中,△H1<△H2是( )
A、C(s)+
| ||||
B、
| ||||
| C、2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | ||||
| D、S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2 |
下列关于反应能量的说法正确的是( )
| A、Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s);△H=-216kJ/mol,E反应物>E生成物 | ||||
| B、CaCO3(s)=CaO(s)+CO2(g);△H=+178.5kJ/mol,E反应物>E生成物 | ||||
C、HI(g)?
| ||||
| D、H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,含1molNaOH水溶液与含0.5mol H2SO4的浓硫酸混合后放热57.3 kJ |
FeCl3溶液和Fe(OH)3胶体的共同性质是( )
| A、都能产生丁达尔效应现象 |
| B、都能透过半透膜 |
| C、通常情况下均稳定透明 |
| D、分散质粒子直径都是1~100nm |
能正确表示下列反应的离子方程式是( )
| A、浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B、明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
| C、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| D、Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |