题目内容
下列叙述正确的是( )
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等 |
| C、14g一氧化碳气体一定比20 g氧气的体积小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等 |
考点:物质的量的相关计算
专题:
分析:A.应描述为同温同压下,相同体积的气体的物质的量一定相等;
B.物质的量相等的甲烷与CO含有分子数目相等;
C.二者物质的量可以确定,但温度、压强会影响气体的体积;
D.同温同压下,气体体积相等,则气体物质的量相等,含有分子数目相等.
B.物质的量相等的甲烷与CO含有分子数目相等;
C.二者物质的量可以确定,但温度、压强会影响气体的体积;
D.同温同压下,气体体积相等,则气体物质的量相等,含有分子数目相等.
解答:
解:A.同温同压下,相同体积的气体的物质的量一定相等,不是气体物质的量则不一定相等,故A错误;
B.根据N=nNA可知,物质的量相等的甲烷与CO含有分子数目相等,故B错误;
C.根据n=
可以计算二者物质的量,但温度、压强会影响气体的体积,CO、氧气所处温度、压强不确定,不能确定二者体积大小,故C错误;
D.同温同压下,气体体积相等,则气体物质的量相等,含有分子数目相等,故D正确,
故选D.
B.根据N=nNA可知,物质的量相等的甲烷与CO含有分子数目相等,故B错误;
C.根据n=
| m |
| M |
D.同温同压下,气体体积相等,则气体物质的量相等,含有分子数目相等,故D正确,
故选D.
点评:本题考查物质的量有关计算、阿伏伽德罗定律等,难度不大,注意根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
相关题目
常温下,下列溶液中的粒子浓度关系正确的是( )
| A、0.2mol?L-1HF溶液与0.1mol?L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(F-)-c(HF) |
| B、0.1mol?L-1KHCO3溶液中:c(CO32-)+c(OH-)=c(H+)+2c(H2CO3) |
| C、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH+)>c(OH-)=c(H+) |
| D、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
室温下向浓度均为0.1mol?L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示.下列说法正确的是( )


| A、G点时沉淀的质量为18.5g |
| B、该混合溶液中6c(Fe3+)>c(NO3-) |
| C、该混合溶液在空气中加热、蒸干、灼烧后所得到的固体为Fe(NO3)3和Al(NO3)3 |
| D、室温下Ksp[Al(OH)3]>Ksp[Fe(OH)3] |
下列在溶液中可以大量共存的一组离子是( )
| A、K+、SO42-、Cu2+、NO3- |
| B、Fe3+、Na+、I-、HCO3- |
| C、Mg2+、H+、SiO32-、SO42- |
| D、K+、NH4+、OH-、SO42- |
用nA表示阿伏伽德罗常数的值.下列说法正确的是( )
| A、28g N2中含有氮原子数为nA |
| B、1molNa与足量O2反应转移的电子数为nA |
| C、常温常压下,22.4LCO2中含有的分子数为nA |
| D、1mol?L-1K2SO4溶液中含有的钾离子数为nA |
胶体区别于其它分散系的实质是( )
| A、胶体粒子直径在1nm-100nm之间 |
| B、胶体可发生丁达尔效应 |
| C、胶体粒子不能透过半透膜 |
| D、胶体粒子能够发生布朗运动 |

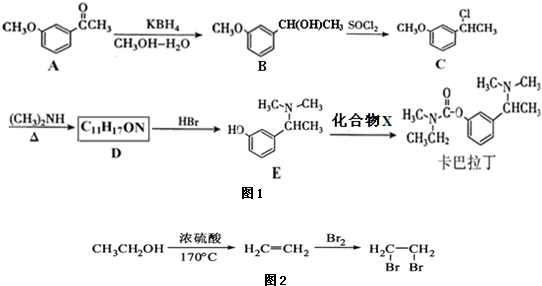
 )和丙酮(
)和丙酮( )制备化合物
)制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图如图2:
的合成路线流程图(无机试剂任选).合成路线流程图如图2: