题目内容
向0.2mol?L-1的NaOH溶液中通入CO2,溶液中阴离子浓度与通入CO2的物质的量关系符合图中的( )
A、 |
B、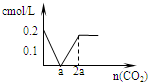 |
C、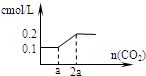 |
D、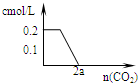 |
考点:离子方程式的有关计算
专题:
分析:未通入CO2,溶液中阴离子浓度为0.2mol?L-1OH-,CO2通入NaOH溶液中可能发生的反应有:CO2+2NaOH=Na2CO3+H20,CO2+Na2CO3+H20=2NaHCO3,二者恰好反应时,产物为Na2CO3,当CO2过量时,产物为NaHCO3,以此判断.
解答:
解:CO2通入NaOH溶液中可能发生的反应有:CO2+2NaOH=Na2CO3+H20,CO2+Na2CO3+H20=2NaHCO3,
向0.2mol?L-1的NaOH溶液中通入CO2,假设溶液的体积为1L,未通入CO2,溶液中阴离子浓度为0.2mol?L-1OH-,
通入0.1molCO2,此时发生CO2+2NaOH=Na2CO3+H20,生成0.1molNa2CO3,溶液中阴离子浓度为0.1mol?L-1CO32-,a为0.1molCO2,
继续通入CO2,此时发生CO2+Na2CO3+H20=2NaHCO3,2a为0.2molCO2,溶液中阴离子浓度为0.2mol?L-1HCO3-,图中A符合,
故选A.
向0.2mol?L-1的NaOH溶液中通入CO2,假设溶液的体积为1L,未通入CO2,溶液中阴离子浓度为0.2mol?L-1OH-,
通入0.1molCO2,此时发生CO2+2NaOH=Na2CO3+H20,生成0.1molNa2CO3,溶液中阴离子浓度为0.1mol?L-1CO32-,a为0.1molCO2,
继续通入CO2,此时发生CO2+Na2CO3+H20=2NaHCO3,2a为0.2molCO2,溶液中阴离子浓度为0.2mol?L-1HCO3-,图中A符合,
故选A.
点评:本题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正确的分析各个反应的过程,并结合图象分析问题,抓住“三点一趋势”(起点、拐点、终点和图象的变化趋势),对培养学生分析问题的能力有一定帮助,题目难度中等.

练习册系列答案
相关题目
能将化学能转化为电能的装置(烧杯中溶液均为稀硫酸)是( )
A、 |
B、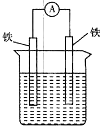 |
C、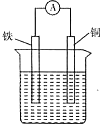 |
D、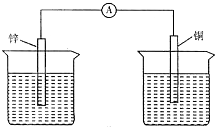 |
下列各组物质混合后,不能生成NaOH的是( )
| A、Na与水 |
| B、Na2O2与水 |
| C、Ca(OH)2溶液和Na2CO3溶液 |
| D、Fe(OH)3和NaCl溶液 |
下列叙述正确的是( )
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等 |
| C、14g一氧化碳气体一定比20 g氧气的体积小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、1.7 g羟基所含电子的数目为NA |
| B、0.1 mol丙烯醛中含有双键的数目为O.1NA |
| C、室温时,pH=13的1.0 L Ba(OH)2溶液中含有OH-的数目为0.2NA |
| D、标准状况下,7.8 g苯中含氢原子的数目为O.6NA |
 某校化学兴趣小组拟用浓盐酸与二氧化锰加热反应,制取并收集2瓶干燥.纯净的氯气.为防止换集气瓶时生成的氯气污染空气,设计了如下装置:
某校化学兴趣小组拟用浓盐酸与二氧化锰加热反应,制取并收集2瓶干燥.纯净的氯气.为防止换集气瓶时生成的氯气污染空气,设计了如下装置: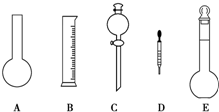 碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:
碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作: