题目内容
常温下,下列溶液中的粒子浓度关系正确的是( )
| A、0.2mol?L-1HF溶液与0.1mol?L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(F-)-c(HF) |
| B、0.1mol?L-1KHCO3溶液中:c(CO32-)+c(OH-)=c(H+)+2c(H2CO3) |
| C、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH+)>c(OH-)=c(H+) |
| D、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.反应后的溶质为等浓度的NaF和氟化氢,根据混合液中的电荷守恒和物料守恒判断;
B.溶液中满足质子守恒,根据碳酸氢钾溶液中的质子守恒判断;
C.氨水为弱碱,混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+);
D.溶液中还存在氢离子,电荷守恒中漏掉了氢离子.
B.溶液中满足质子守恒,根据碳酸氢钾溶液中的质子守恒判断;
C.氨水为弱碱,混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+);
D.溶液中还存在氢离子,电荷守恒中漏掉了氢离子.
解答:
解:A.0.2mol?L-1HF溶液与0.1mol?L-1NaOH溶液等体积混合,混合后的溶质为等浓度的NaF和HF,根据电荷守恒可得:①c(Na+)+c(H+)=c(OH-)+c(F-),根据物料守恒可得:②2c(Na+)=c(F-)+c(HF),②×2带人①可得:2c(H+)-2c(OH-)=c(F-)-c(HF),故A正确;
B.0.1mol?L-1KHCO3溶液中,根据质子守恒可得:c(OH-)=c(H+)+c(H2CO3),由于碳酸根离子的水解程度大于其电离程度,则c(H2CO3)>c(CO32-),所以c(CO32-)+c(OH-)<c(H+)+2c(H2CO3),故B错误;
C.氨水为弱碱,pH=11的氨水的浓度大于0.001mol/L,pH=3的盐酸增大浓度为0.001mol/L,两溶液等体积混合后氨水过量,溶液显示碱性,则:c(OH-)>c(H+),根据电荷守恒可知c(Cl-)<c(NH4+),所以溶液中离子浓度关系为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故C错误;
D.新制氯水中加入固体NaOH,根据电荷守恒可得:c(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-),故D错误;
故选A.
B.0.1mol?L-1KHCO3溶液中,根据质子守恒可得:c(OH-)=c(H+)+c(H2CO3),由于碳酸根离子的水解程度大于其电离程度,则c(H2CO3)>c(CO32-),所以c(CO32-)+c(OH-)<c(H+)+2c(H2CO3),故B错误;
C.氨水为弱碱,pH=11的氨水的浓度大于0.001mol/L,pH=3的盐酸增大浓度为0.001mol/L,两溶液等体积混合后氨水过量,溶液显示碱性,则:c(OH-)>c(H+),根据电荷守恒可知c(Cl-)<c(NH4+),所以溶液中离子浓度关系为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故C错误;
D.新制氯水中加入固体NaOH,根据电荷守恒可得:c(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-),故D错误;
故选A.
点评:本题考查溶液中离子浓度大小比较、酸碱混合的定性判断,题目难度中等,注意明确物料守恒、电荷守恒、质子守恒的含义,明确酸碱混合的定性判断方法,选项C为易错点,注意弱电解质部分电离的特点.

练习册系列答案
相关题目
据报道用Mg与石墨作电极与NH4Cl溶液形成原电池(盐桥为装有琼胶的饱和KCl溶液),也可生成NH3.下列说法正确是( )
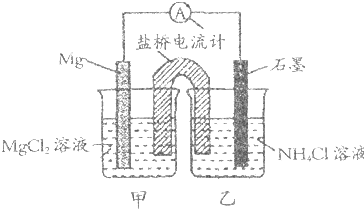

| A、石墨电极反应式为2NH4++2e-=2NH3↑+H2↑ |
| B、乙烧杯中一直存在:c(Cl-)<c(NH4+) |
| C、电子流向是由石墨→导线→Mg |
| D、盐桥中的Cl-移向乙烧杯 |
常温下,下列有关电解质溶液微粒关系比较正确的是( )
| A、氨水和氯化铵的混合液,当pH=7时,c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的NaOH溶液等体积混合,混合液中c(H+)不一定等于c(OH-) |
| C、0.1mol/L的Na2CO3溶液中:c(Na+)=c(H2CO3)+c(HCO3-)+2c(CO32-) |
| D、PH=3的H2SO4和NaCl溶液中,一定存在c(Na+)=c(Cl-) |
25℃时,已知弱酸的电离常数:Ki(CH3COOH)=1.8×10-5;Ki1(H2CO3)=4.4×10-7;Ki2(H2CO3)=4.7×10-11;Ki(HClO)=4.0×10-8.则下列说法正确的是( )
| A、物质的量浓度相等的溶液pH关系:pH(NaClO)>pH(Na2CO3)>pH(CH3COONa) |
| B、向NaClO溶液中通少量CO2:CO2+NaClO+H2O→NaHCO3+HClO |
| C、a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则a一定小于b |
| D、向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度 |
能将化学能转化为电能的装置(烧杯中溶液均为稀硫酸)是( )
A、 |
B、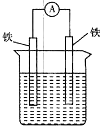 |
C、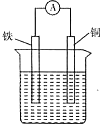 |
D、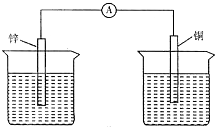 |
下列叙述正确的是( )
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等 |
| C、14g一氧化碳气体一定比20 g氧气的体积小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等 |

 如图在下衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴KBr溶液,品红溶液,含有酚酞的澄清石灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿.提示:实验室中所用的少量氯气可以用下述原理制取:
如图在下衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴KBr溶液,品红溶液,含有酚酞的澄清石灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿.提示:实验室中所用的少量氯气可以用下述原理制取: