题目内容
4.核素钬67166Ho的中子数为( )| A. | 166 | B. | 99 | C. | 67 | D. | 32 |
分析 67166Ho中质子数为67,质量数为166,中子数=质量数-质子数,据此分析解答.
解答 解:67166Ho中质子数为67,质量数为166,中子数=质量数-质子数=166-67=99,故选B.
点评 本题考查了质量数、质子数和中子数之间的关系,难度不大,明确原子中数字的意义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列说法正确的是( )
| A. | 标准状况下,1mol水的体积约是22.4升 | |
| B. | 1molH2所占的体积约是22.4升 | |
| C. | 标准状况下,6.02×1023个分子所占的体积约是22.4升 | |
| D. | 标准状况下,28g氮气和CO的混合气体的体积约是22.4升 |
12.下列物质递变规律不能用元素周期律解释的是( )
| A. | 金属性:Na>Mg | B. | 热稳定性:HF>HCl | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 氧化性:O2>S |
9.下列说法正确的是( )
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 氧化铜和氧化亚铜都是黑色固体 | |
| C. | 铝在高温下能还原锰、铁、铬等金属氧化物得到金属 | |
| D. | 因为镁和铝在空气中都能形成氧化膜,所以镁铝都不能溶于浓盐酸 |
16.短周期元素X、Y、W、Q在元素周期表中位置如图所示.下列说法正确的是( )
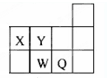

| A. | 元素X与元素Y可形成多种化合物 | |
| B. | 原子半径的大小顺序为:X>Y>W>Q | |
| C. | 还原性:W2-<Q- | |
| D. | 元素W的最高价氧化物对应水化物的酸性比Q的强 |
13.如图是课外活动小组设计的化学电源使LED灯发光的装置.下列说法不正确的是( )
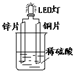

| A. | 锌片换成铁片,电路中的电流方向不变 | |
| B. | 铜电极的电极反应式为Cu2++2e-=Cu | |
| C. | 将硫酸换成柠檬汁,导线中仍有电子流动 | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
6.下列说法正确的是( )
| A. | 只含离子键的化合物称为离子化合物 | |
| B. | 化学键不仅存在于原子间,也存在于分子间 | |
| C. | 原子间通过极性键结合成分子的物质,一定是共价化合物 | |
| D. | 不同元素组成的多原子分子里的化学键一定是极性键 |