题目内容
13.如图是课外活动小组设计的化学电源使LED灯发光的装置.下列说法不正确的是( )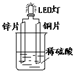
| A. | 锌片换成铁片,电路中的电流方向不变 | |
| B. | 铜电极的电极反应式为Cu2++2e-=Cu | |
| C. | 将硫酸换成柠檬汁,导线中仍有电子流动 | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
分析 A.Zn、Cu和稀硫酸及Fe、Cu和稀硫酸都能构成原电池,且这两个原电池中都是Cu作正极,原电池放电时,电流从正极沿导线流向负极;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气;
C.柠檬汁溶液呈酸性,Zn、Cu和柠檬汁能构成原电池;
D.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光.
解答 解:A.原电池放电时,电流从正极沿导线流向负极,Zn、Cu和稀硫酸及Fe、Cu和稀硫酸都能构成原电池,且这两个原电池中都是Cu作正极,Zn或Fe作负极,所以锌片换成铁片,电路中的电流方向不变,故A正确;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气,电极反应式为2H++2e-=H2↑,故B错误;
C.柠檬汁溶液呈酸性,Zn、Cu和柠檬汁能构成原电池,所以将硫酸换成柠檬汁,导线中仍有电子流动,故C正确;
D.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光,则装置中存在“化学能→电能→光能”的转换,故D正确;
故选B.
点评 本题考查化学电源新型电池,为高频考点,侧重考查学生分析判断能力,明确原电池原理、正负极判断方法、正负极上发生的反应是解本题关键,会正确书写电极反应式,题目难度不大.

练习册系列答案
相关题目
4.核素钬67166Ho的中子数为( )
| A. | 166 | B. | 99 | C. | 67 | D. | 32 |
1.下列有关氰酸铵(NH4CNO)与尿素[CO(NH2)2]的说法正确的是( )
| A. | 都是共价化合物 | B. | 都是离子化合物 | C. | 互为同分异构体 | D. | 互为同系物 |
8.下列仪器中一般不能用作反应容器的是( )
| A. | 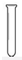 | B. | 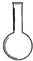 | C. | 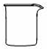 | D. | 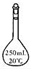 |
18.下列工业过程需要石灰石作为原料的是( )
| A. | 氯碱工业 | B. | 高炉炼铁 | C. | 粗硅提纯 | D. | 硫酸工业 |
2.下列离子组在一定条件下能大量共存,且加入相应试剂后发生反应的离子方程式正确的是( )
| 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 | |
| A | K+、AlO2-、NO3- | 过量CO2 | CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- |
| B | ClO-、Fe3+、I- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| C | Ca2+、Na+、OH- | NaHCO3溶液 | HCO3-+OH-═CO32-+H2O |
| D | NH4+、HCO3-、Cl- | NaOH溶液 | NH4++HCO3-+2OH-═CO32-+NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关能源的说法正确的是( )
| A. | 二氧化硅是人类将太阳能转化为电能的常用材料 | |
| B. | 氢氧燃料电池的能量转换率可达100%,是一种具有应用前景的绿色能源 | |
| C. | 设法将太阳光聚焦产生高温,使水分解产生氧气,是开发氢能的研究方向之一 | |
| D. | 原电池是把化学能直接转化为电能的装置,所以由原电池提供的电能是一次能源 |

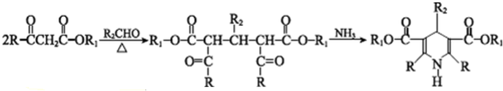
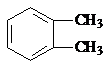 $→_{光}^{氯气}$
$→_{光}^{氯气}$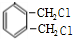 $→_{△}^{氢氧化钠溶液}$
$→_{△}^{氢氧化钠溶液}$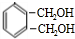 $→_{催化剂}^{氧气}$
$→_{催化剂}^{氧气}$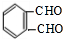 .
.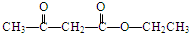 .
.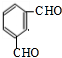 .
.