题目内容
19.在醛、酮中,其他碳原子按与羰基相连的顺序,依次叫α,β,γ,…碳原子,如: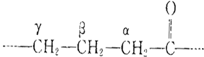
在稀碱或稀酸的作用下,2分子含有α-氢原子的醛能自身加成生成1分子β-羟基醛,如:

巴豆酸(CH3-CH=CH-COOH)主要用于有机合成制合成树脂或作增塑剂.现应用乙醇和其他无机原料合成巴豆酸.请写出各步反应的化学方程式2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O、2CH3CHO$\stackrel{OH-}{→}$ CH3CH(OH)CH2CHO、CH3CH(OH)CH2CHO+O2$→_{△}^{Cu或Ag}$CH3COCH2COOH+H2O、CH3COCH2COOH+H2$→_{△}^{Ni}$CH3CH(OH)CH2COOH、CH3CH(OH)CH2COOH$→_{△}^{浓硫酸}$CH3-CH=CH-COOH+H2O.
分析 巴豆酸(CH3-CH=CH-COOH),含有4个碳原子,用乙醇和其他无机原料合成巴豆酸,需2分子的乙醇,乙醇催化氧化生成乙醛和水,利用在稀碱或稀酸的作用下,2分子含有α-氢原子的醛能自身加成生成1分子β-羟基醛,增长碳链,再氧化醛基、醇羟基,得到含有羧基、羰基的四碳有机物,催化加氢,使羰基变成醇羟基,醇羟基与相邻的碳脱水形成巴豆酸,据此分析书写各步反应方程式.
解答 解:用乙醇和其他无机原料合成巴豆酸:
乙醇催化氧化生成乙醛和水,其反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,
在稀碱作用下,2分子含有α-氢原子的乙醛能自身加成生成1分子β-羟基醛,其反应方程式为:2CH3CHO$\stackrel{OH-}{→}$ CH3CH(OH)CH2CHO,
醇羟基、醛基催化氧化,其反应方程式为:CH3CH(OH)CH2CHO+O2$→_{△}^{Cu或Ag}$CH3COCH2COOH+H2O,
催化加氢,生成醇,其反应方程式为:CH3COCH2COOH+H2$→_{△}^{Ni}$CH3CH(OH)CH2COOH,
醇羟基消去,其反应方程式为:CH3CH(OH)CH2COOH$→_{△}^{浓硫酸}$CH3-CH=CH-COOH+H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O、2CH3CHO$\stackrel{OH-}{→}$ CH3CH(OH)CH2CHO、CH3CH(OH)CH2CHO+O2$→_{△}^{Cu或Ag}$CH3COCH2COOH+H2O、CH3COCH2COOH+H2$→_{△}^{Ni}$CH3CH(OH)CH2COOH、CH3CH(OH)CH2COOH$→_{△}^{浓硫酸}$CH3-CH=CH-COOH+H2O.
点评 本题以化学方程式书写为载体考查有机物的合成,结合反应信息增长碳链进行推断适解答关键侧重考查分析推理能力,平时需熟练掌握官能团的性质与转化,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 18g重水含有10NA 个电子 | |
| B. | 室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约为3 NA | |
| C. | 常温下0.05 mol•L-1Fe2(S04 ) 3溶液中含Fe 3+数目小于0.1NA | |
| D. | 用惰性电极电解饱和食盐水,当阴极得到2NA个电子时阳极产生22.4 L气体 |
(2)写出下列物质的电子式:①CO2
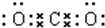 ;②NaOH
;②NaOH .
.(3)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
②元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH.
③呈两性的氢氧化物是Al(OH)3,其与③的最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+H2O.
④在③~⑦元素中,原子半径最大的是Na.
| A. | CO2分子比例模型: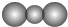 | |
| B. | 中子数为21的钾原子:4019K | |
| C. | NH4I的电子式: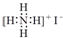 | |
| D. | HCO3-的电离方程式:HCO3-+H2O?H3O++CO32- |
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | CO2通入NaClO溶液中能生成HClO |
| B | 根据溶液的pH与溶液酸碱性的关系 | pH=6.8的溶液一定显酸性 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 同主族元素从上至下非金属性减弱 | HF、HCl、HBr、HI的酸性依次减弱 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 166 | B. | 99 | C. | 67 | D. | 32 |
| A. | 升温 | B. | 改用粉末状大理石 | ||
| C. | 加入一定量水 | D. | 加入适量浓盐酸 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 共价键一定存在于共价化合物中,也可能存在于离子化合物中 | |
| B. | Na2O2中既含有离子键也含有极性共价键 | |
| C. | NH4Cl是都由非金属元素组成的既含有离子键也含有共价键的离子化合物 | |
| D. | 熔化状态下不导电的化合物一定是共价化合物 |