题目内容
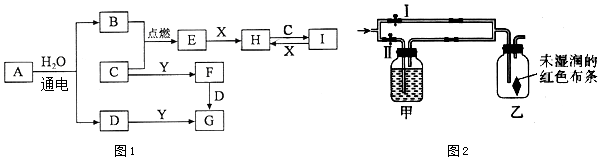
16. A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去).
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去).(1)若A是一种淡黄色单质固体,则B→C的化学方程式为2SO2+O2 $\frac{\underline{催化剂}}{△}$2SO3 .
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为过氧化钠,试用化学方程式表示该物质的一个重要应用2Na2O2+2H2O═4NaOH+O2↑、2Na2O2+2CO2═2Na2CO3+O2.
(3)若C是红棕色气体,则A的化学式可能为N2 或NH3,试写出C与水反应的化学方程式3NO2+H2O═2HNO3+NO.
分析 (1)A是一种黄色单质固体,应为S,则B为SO2,C为SO3;
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2;
(3)若C是红棕色气体,则A为N2或NH3,B为NO,C为NO2.
解答 解:(1)A是一种黄色单质固体,应为S,则B为SO2,C为SO3,B→C的化学方程式为:2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,
故答案为:2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3 ;
(2)A是一种活泼金属,C是淡黄色固体,则A为Na,B为Na2O,C为Na2O2,应用为2Na2O2+2H2O═4NaOH+O2↑、2Na2O2+2CO2═2Na2CO3+O2,作供氧剂,
故答案为:过氧化钠;2Na2O2+2H2O═4NaOH+O2↑、2Na2O2+2CO2═2Na2CO3+O2;
(3)若C是红棕色气体,则A为N2或NH3,B为NO,C为NO2,C与水反应的化学方程式为:3NO2+H2O═2HNO3+NO,
故答案为:N2 或NH3;3NO2+H2O═2HNO3+NO.
点评 本题考查无机物的推断,题目难度中等,本题注意根据物质的颜色判断物质的可能性,注意知识积累.

练习册系列答案
相关题目
6.某温度下,相同pH的硫酸和硫酸铝溶液中由水电离出的c(H+)分别是l.0×l0-10mol/L和1.0×10-3 mol/L,则此温度下水的离子积Kw为( )
| A. | 1.0×l0-15 | B. | 1.0×10-14 | C. | 1.0×10-13 | D. | l.0×l0-7 |
7.合成高分子化合物提高了人类的生活质量.下列说法正确的是( )
| A. | 涤纶、锦纶、蚕丝都属于合成纤维 | |
| B. | 塑料、液晶高分子和合成橡胶被称为三大合成材料 | |
| C. | 用于生产“尿不湿”的高吸水性树脂属于功能高分子材料 | |
| D. | 酚醛树脂是酚类物质和醛类物质加聚而成的高分子化合物 |
4.生活中的化学知识无处不在,下列化学知识的应用错误的是( )
| A. | 明矾可以除去水中的悬浮颗粒等杂质,所以可以作净水剂 | |
| B. | 可用燃烧的方法鉴别羊毛围巾和合成纤维围巾 | |
| C. | 黄瓜含有丰富的维生素C,热锅爆炒可以减少维生素C的流失 | |
| D. | 石英玻璃纤维传导光的能力非常强,所以常用于制作光纤 |
1.下列关于指定粒子构成的描述中,不正确的是( )
| A. | 14Cl与16O具有相同的中子数 | |
| B. | ${\;}_{50}^{119}Sn$与${\;}_{82}^{207}Pb$具有相同最外层电子数 | |
| C. | NH4+与OH-具有相同的质子数和电子数 | |
| D. | O22-和S2-具有相同的质子数和电子数 |
8.下列各项操作中,能出现“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2 ②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀氢氧化钠溶液 ④向硅酸钠溶液中逐滴加入过量的盐酸.
①向饱和碳酸钠溶液中通入过量的CO2 ②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀氢氧化钠溶液 ④向硅酸钠溶液中逐滴加入过量的盐酸.
| A. | ①②③ | B. | ②③ | C. | ②④ | D. | ①③ |
5.下列物质的俗称表示同一物质的是( )
| A. | 明矾、胆矾 | B. | 冰、干冰 | C. | 火碱、烧碱 | D. | 苏打、小苏打 |
6.常温下,下列有关电解质溶液的说法,正确的是( )
| A. | 1mol/L的CH3COOH溶液和0.1mol/L的CH3COOH溶液,水的电离程度前者大于后者 | |
| B. | pH=2的HA溶液和pH=12的NaOH溶液等体积混合后溶液显碱性,则混合后的溶液中存在平衡:A-+H2O?HA+OH- | |
| C. | 已知同浓度的NaA、NaB、NaX溶液碱性逐渐增强,则Ks(HA)<Ks(HB)<Ks(HX) | |
| D. | 已知常温下AgCl的Ksp=1.56×10-10,则浓度均为2.2×10-5mol/L的AgNO3溶液、NaCl溶液等体积混合,会产生AgCl白色沉淀 |
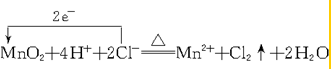 .
.