题目内容
下列有关实验的叙述中,合理的是( )


| A、把SO2通入紫色石蕊试液,可验证SO2的漂白性 |
| B、构成如图所示装置时,盐桥中的K+向左池移动 |
| C、配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高 |
| D、将10克ZnSO4?7H2O溶解在90克水中配制10%的ZnSO4溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.二氧化硫不能漂白酸碱指示剂;
B.盐桥中阳离子向正极移动;
C.根据c=
判断误差;
D.ZnSO4?7H2O溶于水后,溶液中的溶质是硫酸锌.
B.盐桥中阳离子向正极移动;
C.根据c=
| n |
| V |
D.ZnSO4?7H2O溶于水后,溶液中的溶质是硫酸锌.
解答:
解:A.二氧化硫具有漂白性,能使品红溶液褪色,但不能使酸碱指示剂褪色,故A错误;
B.该装置构成原电池,锌易失电子作负极,铜作正极,盐桥中钾离子向正极电池即右池移动,故B错误;
C.根据c=
知,定容时俯视容量瓶的刻度线,导致溶液体积偏小,则配制溶液浓度偏高,故C正确;
D.ZnSO4?7H2O溶于水后,溶液中的溶质是硫酸锌,所以将10克ZnSO4?7H2O溶解在90克水中配制的溶液中,硫酸锌浓度小于10%,故D错误;
故选C.
B.该装置构成原电池,锌易失电子作负极,铜作正极,盐桥中钾离子向正极电池即右池移动,故B错误;
C.根据c=
| n |
| V |
D.ZnSO4?7H2O溶于水后,溶液中的溶质是硫酸锌,所以将10克ZnSO4?7H2O溶解在90克水中配制的溶液中,硫酸锌浓度小于10%,故D错误;
故选C.
点评:本题考查较综合,涉及二氧化硫的漂白性、溶液的配制、原电池原理等知识点,根据原电池原理、c=
、二氧化硫的漂白性等知识点来分析解答即可,易错选项是A,注意二氧化硫的漂白性和次氯酸的漂白性不同,二氧化硫能漂白品红溶液但不能漂白酸碱指示剂,次氯酸能漂白酸碱指示剂,为易错点.
| n |
| V |

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列离子方程式正确的是( )
| A、碳酸氢钠的电离:NaHCO3=Na++HCO3- |
| B、将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑ |
| C、硫化钠水解:S2-+2H2O=H2S↑+2OH- |
| D、向氯化铝溶液中加入过量的氨水:Al3++4OH-=Al(OH )4- |
在月球上发现水被美国《科学》杂志评为2009年十大科学突破之一.下列化学反应中水作还原剂的是( )
| A、CaO+H2O=Ca(OH)2 |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、Cl2+2H2O=HCl+HClO |
| D、2F2+2H2O=4HF+O2 |
常温下,某无色溶液中由水电离出来的c(H+)=1×10-12 mol?L-1,该溶液中一定能大量存在的离子组是( )
| A、Na+、K+、MnO4-、SO42- |
| B、Mg2+、NH4+、SO42-、Cl- |
| C、Na+、Cl-、NO3-、SO42- |
| D、Na+、K+、CO32-、NO3- |
NA代表阿伏加德罗常数.下列有关叙述正确的是( )
| A、标准状况下,2.24LH2O含有的分子数等于0.1NA |
| B、20g重水(D2 O)所含的电子数为10NA |
| C、标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA |
| D、25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
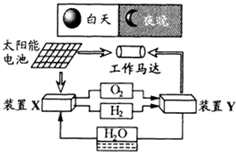 如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )
如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )| A、二氧化硅是太阳能电池的光电转换材料 |
| B、装置Y中正极的电极反应式为:O2+2H2O+4e-=4OH- |
| C、装置X能实现燃料电池的氢气和氧气再生 |
| D、装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |