题目内容
20.某学习小组通过下列装置探究MnO2与FeCl3•6H2O能否反应产生Cl2.资料显示:氯化铁为共价化合物.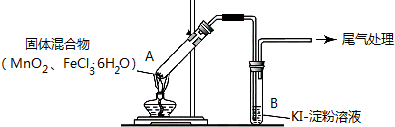
实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
(2)分析现象 ii,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3•6H2O,产生白雾和黄色气体.
b.用KSCN 溶液分别检验现象 ii 和a 中的黄色气体,溶液均变红.
通过该实验说明现象 ii 中黄色气体含有FeCl3.
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b 检出的气体使之变蓝,反应的离子方程式是2Fe3++2I-=2Fe2++I2.实验证实推测成立.
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝.通过进一步实验确认了这种可能性,其实验方案是另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立.
(4)为进一步确认黄色气体是否含有 Cl2,小组提出两种方案,均证实了Cl2的存在.
| 方案1 | 在A、B间增加盛有某种试剂的洗气瓶C | B中溶液变为蓝色 |
| 方案2 | 将B中KI淀粉溶液替换为NaBr溶液;检验 Fe2+ | B中溶液呈浅橙红色;未检出Fe2+ |
②方案2 中检验 Fe2+的原因是排除Fe3+将Br-氧化成Br2 的可能性.
(5)将A中产物分离得到Fe2O3和MnCl2,A中发生反应的化学方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.
分析 (1)FeCl3•6H2O 受热失去结晶水,同时水解,生成HCl气体,HCl和H2O结合形成盐酸小液滴;
(2)FeCl3溶液中滴入KSCN溶液,发生络合反应,用KSCN 溶液检验现象ii 和A 中的黄色气体,溶液均变红,说明含有FeCl3;
(3)①氯化铁具有强氧化性,可以将碘离子氧化为碘单质;
②作对照实验,需要除去Cl2 和Fe3+的干扰才能检验酸性情况下的O2 影响,所以最好另取溶液对酸性情况下氧气的影响进行检验.因为原题中存在HCl气体,所以酸化最好选用盐酸;
(4)①方案1:除去Cl2中的FeCl3 和O2(H+),若仍能观察到B中溶液仍变为蓝色,则证明原气体中确实存在Cl2,Cl2 中的氯化氢的去除使用饱和NaCl溶液,饱和NaCl溶液也可以让FeCl3 溶解,并且除去O2 影响过程中提供酸性的HCl气体,从而排除两个其他影响因素;
②方案2:若B中观察到浅橙红色,则证明有物质能够将Br-氧化成Br2,若未检查到Fe2+,则证明是Cl2 氧化的Br-,而不是Fe3+.另外,因为还原剂用的不是I-,可不用考虑O2(H+)的影响问题;
(5)二氧化锰与FeCl3•6H2O 反应生成Fe2O3、MnCl2、Cl2及水,据此结合原子守恒书写化学方程式.
解答 解:(1)FeCl3•6H2O 受热失去结晶水FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeCl3+6H2O,同时水解FeCl3+3H2O?Fe(OH)3+3HCl,生成HCl气体,HCl和H2O结合形成盐酸小液滴,而形成白雾,
故答案为:HCl小液滴;FeCl3•6H2O 受热水解,生成HCl 气体,同时受热失去结晶水,HCl和H2O 结合形成盐酸小液滴;
(2)FeCl3溶液中滴入KSCN溶液,发生络合反应,Fe3++3SCN-=Fe(SCN)3,生成血红色的硫氰化铁,用KSCN 溶液检验现象ii 和A 中的黄色气体,溶液均变红,说明含有FeCl3,
故答案为:FeCl3;
(3)①碘离子具有还原性,氯化铁具有强氧化性,两者反应,碘离子被氧化为碘单质,反应离子方程式为:2Fe3++2I-=2Fe2++I2,
故答案为:2Fe3++2I-=2Fe2++I2;
②FeCl3•6H2O 受热水解,生成HCl气体,作对照实验,需用盐酸酸化,另取一支试管,向其中加入KI-淀粉溶液,再滴入几滴HCl溶液,在空气中放置,观察一段时间后溶液是否变蓝,若一段时间后溶液变蓝则推测成立,
故答案为:另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立;
(4)①方案1:氯化铁能氧化碘离子,氧气在酸性条件下,能氧化碘离子,所以需除去Cl2中的FeCl3 和O2(H+),若仍能观察到B中溶液仍变为蓝色,则证明原气体中确实存在Cl2,使用饱和NaCl溶液,可以让FeCl3 溶解,并且除去O2 影响过程中提供酸性的HCl气体,从而排除两个其他影响因素,
故答案为:饱和NaCl溶液;
②方案2:若B中观察到浅橙红色,为溴水的颜色,则证明有物质能够将Br-氧化成Br2,铁离子不能氧化溴离子,若未检查到Fe2+,则证明是Cl2氧化的Br-,而不是Fe3+.另外,因为还原剂用的不是I-,可不用考虑O2(H+)的影响问题,
故答案为:排除Fe3+将Br-氧化成Br2 的可能性;
(5)二氧化锰与FeCl3•6H2O 反应生成Fe2O3、MnCl2、Cl2及水,反应方程式为:3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O,
故答案为:3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.
点评 本题考查物质性质探究实验,侧重对原理分析、陌生方程式的书写等考查,是对学生综合能力的考查,熟练掌握元素化合物性质,题目难度中等.

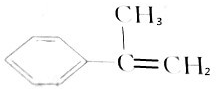 ,则该有机物与氢气完全反应后产物的一氯代物的结构有( )
,则该有机物与氢气完全反应后产物的一氯代物的结构有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
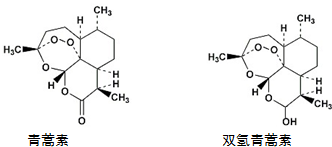
| A. | 青蒿素能发生还原反应 | |
| B. | 双氢青蒿素发生酯化反应和氧化反应 | |
| C. | 青蒿素分子中含有过氧键和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
| A. | 若a=b且c(X-)=c(Y-)+c(HY),则HX为强酸 | |
| B. | 若a=b且pH(NaX)>pH(NaY),则c(X-)+c(OH-)>c(Y-)+c(OH-) | |
| C. | 若a>b且c(X-)=c(Y-),则酸性HX>HY | |
| D. | 若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化) |
| A. | 常温常压下,16 g O2和32g O3的混合物中,含有O原子数目为3NA | |
| B. | 标准状况下,1 mol Na2O和1 mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为$\frac{5}{3}$NA |
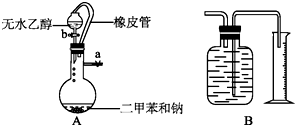 为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.
为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.
 ;
;