题目内容
16.某有机物的结构简式为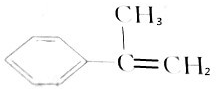 ,则该有机物与氢气完全反应后产物的一氯代物的结构有( )
,则该有机物与氢气完全反应后产物的一氯代物的结构有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
分析 该有机物与氢气完全反应后产物结构简式为: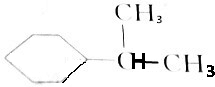 ,依据分子结构中氢原子的不同判断其一氯代物的结构,分子中有6种不同氢原子;
,依据分子结构中氢原子的不同判断其一氯代物的结构,分子中有6种不同氢原子;
解答 解:该有机物与氢气完全反应后产物结构简式为: ,分子中有6种不同氢原子,依据分子结构中氢原子的不同判断其一氯代物的结构有6种,故选A.
,分子中有6种不同氢原子,依据分子结构中氢原子的不同判断其一氯代物的结构有6种,故选A.
点评 本题考查了有机物同分异构体的书写方法和判断方法,注意氢原子的不同时一氯代物的分析依据,掌握基础是解题关键,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
4.将乙烯通入溴的CCl4溶液中.下列说法正确的是( )
| A. | 溶液褪色 | B. | 有沉淀物生成 | C. | 生成物属于烃 | D. | 产物含有双键 |
11.施用氮肥能促进作物生长,并能提高作物中蛋白质的含量.下列关于氮肥的说法错误的是( )
| A. | 尿素CO(NH2)2是一种氮肥 | |
| B. | 储存碳酸氢铵时,应密封并置于阴凉通风处 | |
| C. | 铵态氮肥不能与碱性物质如草木灰等混合施用 | |
| D. | 氮肥溶于水,其中的氮元素均以铵离子形式在存 |
1.实验室制取HCl气体的反应原理为:NaCl(固)+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑.则实验室制取下列各组气体时,气体的发生装置与HCl气体相同的是( )
| A. | H2 | B. | CO2 | C. | Cl2 | D. | O2 |
19.下列物质中,含有非极性共价键的离子化合物的是( )
| A. | NH4NO3 | B. | Cl2 | C. | H2O2 | D. | Na2O2 |
20.某学习小组通过下列装置探究MnO2与FeCl3•6H2O能否反应产生Cl2.资料显示:氯化铁为共价化合物.
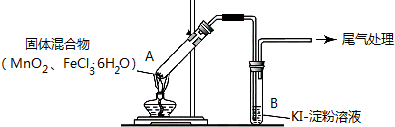
实验操作和现象:
(1)现象i中的白雾是HCl小液滴,形成白雾的原因是FeCl3•6H2O 受热水解,生成HCl 气体,同时受热失去结晶水,HCl和H2O 结合形成盐酸小液滴.
(2)分析现象 ii,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3•6H2O,产生白雾和黄色气体.
b.用KSCN 溶液分别检验现象 ii 和a 中的黄色气体,溶液均变红.
通过该实验说明现象 ii 中黄色气体含有FeCl3.
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b 检出的气体使之变蓝,反应的离子方程式是2Fe3++2I-=2Fe2++I2.实验证实推测成立.
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝.通过进一步实验确认了这种可能性,其实验方案是另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立.
(4)为进一步确认黄色气体是否含有 Cl2,小组提出两种方案,均证实了Cl2的存在.
①方案1 的洗气瓶C中盛放的试剂是饱和NaCl溶液.
②方案2 中检验 Fe2+的原因是排除Fe3+将Br-氧化成Br2 的可能性.
(5)将A中产物分离得到Fe2O3和MnCl2,A中发生反应的化学方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.

实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
(2)分析现象 ii,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3•6H2O,产生白雾和黄色气体.
b.用KSCN 溶液分别检验现象 ii 和a 中的黄色气体,溶液均变红.
通过该实验说明现象 ii 中黄色气体含有FeCl3.
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b 检出的气体使之变蓝,反应的离子方程式是2Fe3++2I-=2Fe2++I2.实验证实推测成立.
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝.通过进一步实验确认了这种可能性,其实验方案是另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立.
(4)为进一步确认黄色气体是否含有 Cl2,小组提出两种方案,均证实了Cl2的存在.
| 方案1 | 在A、B间增加盛有某种试剂的洗气瓶C | B中溶液变为蓝色 |
| 方案2 | 将B中KI淀粉溶液替换为NaBr溶液;检验 Fe2+ | B中溶液呈浅橙红色;未检出Fe2+ |
②方案2 中检验 Fe2+的原因是排除Fe3+将Br-氧化成Br2 的可能性.
(5)将A中产物分离得到Fe2O3和MnCl2,A中发生反应的化学方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.
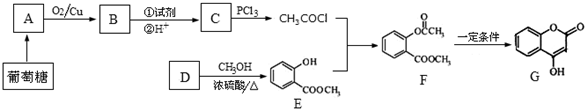
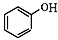 +NaOH→
+NaOH→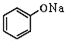 +H2O
+H2O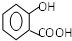 .
.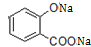 、CH3COONa、CH3OH.
、CH3COONa、CH3OH.

 CH3COOCH2CH3+H2O,酯化(或取代)反应.
CH3COOCH2CH3+H2O,酯化(或取代)反应.