题目内容
已知CO和H2的混合气体称为水煤气,可由碳与水蒸气在高温下反应生成.如图:
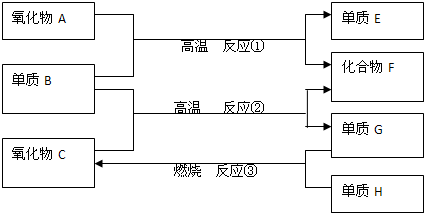
已知:单质E可作为半导体材料,化合物F是有毒的氧化物,常温下C为液态.据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应②的化学方程式是
(4)反应③的化学方程式是 .

已知:单质E可作为半导体材料,化合物F是有毒的氧化物,常温下C为液态.据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应②的化学方程式是
(4)反应③的化学方程式是
考点:无机物的推断
专题:推断题
分析:单质E可作为半导体材料,所以E是硅;C为液态的氧化物,所以C是水;单质G和H反应生成水,则单质G和H,分别是氧气、氢气中的一种;氧化物A和单质B反应生成硅和氧化物F,根据元素守恒知,A是二氧化硅,二氧化硅和单质B反应生成硅和化合物,且F是有毒的氧化物,可推知B是碳,F是一氧化碳,G是氢气,H是氧气,据此解答.
解答:
解:单质E可作为半导体材料,所以E是硅;C为液态的氧化物,所以C是水;单质G和H反应生成水,则单质G和H,分别是氧气、氢气中的一种;氧化物A和单质B反应生成硅和氧化物F,根据元素守恒知,A是二氧化硅;二氧化硅和单质B反应生成硅和化合物,且F是有毒的氧化物,可推知B是碳,F是一氧化碳,G是氢气,H是氧气,
(1)通过以上分析知,A是SiO2,故答案为:SiO2;
(2)通过以上分析知,F是CO,故答案为:CO;
(3)碳和水蒸气在高温下反应生成一氧化碳和氢气,反应方程式为:C+H2O(g)
CO+H2,
故答案为:C+H2O(g)
CO+H2;
(4)氢气在氧气中燃烧生成水,反应方程式为:2H2+O2
2H2O,故答案为:2H2+O2
2H2O.
(1)通过以上分析知,A是SiO2,故答案为:SiO2;
(2)通过以上分析知,F是CO,故答案为:CO;
(3)碳和水蒸气在高温下反应生成一氧化碳和氢气,反应方程式为:C+H2O(g)
| ||
故答案为:C+H2O(g)
| ||
(4)氢气在氧气中燃烧生成水,反应方程式为:2H2+O2
| ||
| ||
点评:本题考查了元素化合物的推断,需要学生熟练掌握元素化合物知识,注意根据题目提供的信息进行推断,难度不大.

练习册系列答案
相关题目
下列物质中不属于电解质的是( )
| A、食盐水 |
| B、BaSO4 |
| C、Na2CO3 |
| D、蔗糖 |
下列物质中不属于电解质的是( )
| A、NaCl |
| B、CO2 |
| C、NaOH |
| D、BaSO4 |
下列变化中,加入还原剂可以实现的是( )
| A、Cu2+→Cu |
| B、SO2→SO3 |
| C、HCl→Cl2 |
| D、NO→NO2 |
下列有关离子方程式的书写正确的是( )
| A、氢氧化铜和盐酸的反应:OH-+H+═H2O |
| B、氧化铜和盐酸的反应:Cu2++2H2O═2 H++Cu(OH)2↓ |
| C、铁与硫酸铜溶液的反应:Fe+Cu2+═Cu+Fe2+ |
| D、铁与稀硫酸的反应:Fe+2H+═Fe3++H2↑ |
下列现象或事实可用同一原理解释的是( )
| A、铁分别加入浓硫酸和氢氧化钠溶液中均无明显现象 |
| B、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
| C、漂白粉溶液和硅酸钠溶液久置空气中都变质 |
| D、SO2既能使品红褪色也能使酸性高锰酸钾褪色 |
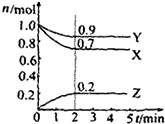 Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
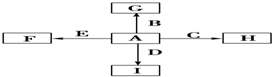
Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下: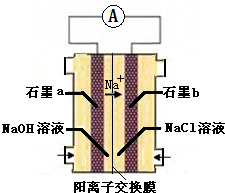 A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D
A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D 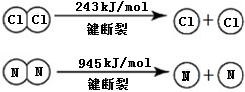 断开1mol H-N键与断开1mol H-Cl键所需能量相差约为
断开1mol H-N键与断开1mol H-Cl键所需能量相差约为