��Ŀ����
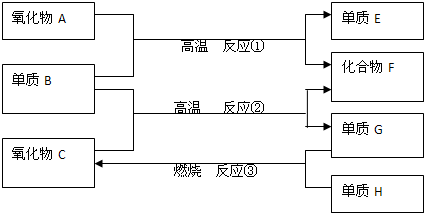
 A��B��C��D����ѧ��ѧ�������������ʣ����ǵ�ת����ϵ���£�A+B=C+D
A��B��C��D����ѧ��ѧ�������������ʣ����ǵ�ת����ϵ���£�A+B=C+D ��1����A��B��C���Ƿǽ����������C�ڿ������ױ��A����A�з���Ԫ�ص���̬�⻯��M�ĵ���ʽΪ
��2����A��D�����ֵ��ʣ�B�Ǻ�ɫ�д��Ե������B�����ᷴӦ������ҺN������N��Һ�еͼ۽��������ӵķ�����
��3��2NH3��g��+3Cl2��g���TN2��g��+6HCl��g��H=-456kJ?mol-1
��֪��
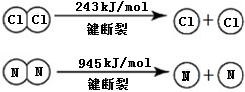 �Ͽ�1mol H-N����Ͽ�1mol H-Cl�������������ԼΪ
�Ͽ�1mol H-N����Ͽ�1mol H-Cl�������������ԼΪ��4��ijѧ���������ͼװ�������Cl2��NH3�ķ�Ӧ������װ����ʵ�����Ŀ�꣬��
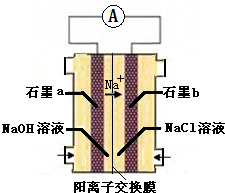
��ʯīb�缫�Ϸ�������
��д��ʯīa�缫�ĵ缫��Ӧʽ��
���㣺������ƶ�,ԭ��غ͵��صĹ���ԭ��
ר�⣺�ƶ���,�绯ѧר��
��������1����A��B��C���Ƿǽ����������C�ڿ������ױ��A��Ӧ��NO��������Ӧ�õ�NO2����CΪNO��AΪNO2��BΪH2O��DΪHNO3��A�з���Ԫ�ص���̬�⻯��MΪNH3��������Nԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ��ǽ�����Խǿ���⻯���ȶ���Խǿ��
��2��B�Ǻ�ɫ�д��Ե������BΪFe3O4��A��D�����ֵ��ʣ���DΪFe��AΪ��ԭ�Ե��ʣ�CΪA�������
N��Һ���еͼ�������ΪFe2+�������軯����Һ���飻��D�ķ�ĩ������ҺN�У�������ӦFe+2Fe3+=3Fe2+��
���Fe�Ļ��ϼ۱仯����ת�Ƶ�����Ŀ��
��3����Ӧ�ʱ�=��Ӧ������ܺ�-����������ܺͣ��ݴ˼��㣻����Խ��ѧ��Խǿ��
��4��װ��Ϊԭ��ط�Ӧ������������b������֪aΪ����������ʧ���ӣ��������������ɵ�����ˮ��bΪ�����������õ��������������ӣ�������ԭ��Ӧ��
��2��B�Ǻ�ɫ�д��Ե������BΪFe3O4��A��D�����ֵ��ʣ���DΪFe��AΪ��ԭ�Ե��ʣ�CΪA�������
N��Һ���еͼ�������ΪFe2+�������軯����Һ���飻��D�ķ�ĩ������ҺN�У�������ӦFe+2Fe3+=3Fe2+��
���Fe�Ļ��ϼ۱仯����ת�Ƶ�����Ŀ��
��3����Ӧ�ʱ�=��Ӧ������ܺ�-����������ܺͣ��ݴ˼��㣻����Խ��ѧ��Խǿ��
��4��װ��Ϊԭ��ط�Ӧ������������b������֪aΪ����������ʧ���ӣ��������������ɵ�����ˮ��bΪ�����������õ��������������ӣ�������ԭ��Ӧ��
���
�⣺��1����A��B��C���Ƿǽ����������C�ڿ������ױ��A��Ӧ��NO��������Ӧ�õ�NO2����CΪNO��AΪNO2��BΪH2O��DΪHNO3��A�з���Ԫ�ص���̬�⻯��MΪNH3��������Nԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ���ԭ����һ�Թ¶Ե��ӣ������ĵ���ʽΪ�� ���ǽ�����O��N�����⻯���ȶ�H2O��NH3��
���ǽ�����O��N�����⻯���ȶ�H2O��NH3��
�ʴ�Ϊ�� ������
������
��2��B�Ǻ�ɫ�д��Ե������BΪFe3O4��A��D�����ֵ��ʣ���DΪFe��AΪ��ԭ�Ե��ʣ�CΪA�������
���������������ᷴӦ����N����Һ�к����Ȼ��������Ȼ�����N��Һ���еͼ�������ΪFe2+���������ӷ���Ϊ��ȡ��Ӧ�����Һ���Թ��У��μ����軯����Һ����Һ������ɫ������������Fe2+��
�����軯����Һ���飻��D�ķ�ĩ������ҺN�У�������ӦFe+2Fe3+=3Fe2+��28gFe�����ʵ���=
=0.5mol����Ӧ��Fe�Ļ��ϼ���0������Ϊ+2��ת�Ƶ������ʵ���=0.5mol��2=1mol��
�ʴ�Ϊ��ȡ��Ӧ�����Һ���Թ��У��μ����軯����Һ����Һ������ɫ������������Fe2+��1��
��3�����ڷ�Ӧ�ʱ�=��Ӧ������ܺ�-����������ܺͣ���6��E��H-N��+3E��Cl-Cl��-6 E��H-Cl��-E��N��N��=-456kJ?mol-1����6��E��H-N��+3��243KJ/mol-6E��H-Cl��-945KJ/mol=-456kJ?mol-1�������õ�E��H-N��-E��H-Cl��=-40KJ/mol���Ͽ�1mol H-N����Ͽ�1mol H-Cl�������������ԼΪ40KJ������Խ��ѧ��Խ�ȶ�����NH3�е�H-N����HCl�е�H-Cl������
�ʴ�Ϊ��40kJ������
��4����װ��Ϊԭ��ط�Ӧ���������Һ���������������ƶ�����ͼ��֪������������b������֪aΪ������bΪ�����������ڵõ��������������ӣ�������ԭ��Ӧ��
�ʴ�Ϊ����ԭ��
��ʯīa�缫Ϊ����������ʧ���ӣ��������������ɵ�����ˮ���缫��ӦʽΪ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
 ���ǽ�����O��N�����⻯���ȶ�H2O��NH3��
���ǽ�����O��N�����⻯���ȶ�H2O��NH3���ʴ�Ϊ��
 ������
��������2��B�Ǻ�ɫ�д��Ե������BΪFe3O4��A��D�����ֵ��ʣ���DΪFe��AΪ��ԭ�Ե��ʣ�CΪA�������
���������������ᷴӦ����N����Һ�к����Ȼ��������Ȼ�����N��Һ���еͼ�������ΪFe2+���������ӷ���Ϊ��ȡ��Ӧ�����Һ���Թ��У��μ����軯����Һ����Һ������ɫ������������Fe2+��
�����軯����Һ���飻��D�ķ�ĩ������ҺN�У�������ӦFe+2Fe3+=3Fe2+��28gFe�����ʵ���=
| 28g |
| 56g/mol |
�ʴ�Ϊ��ȡ��Ӧ�����Һ���Թ��У��μ����軯����Һ����Һ������ɫ������������Fe2+��1��
��3�����ڷ�Ӧ�ʱ�=��Ӧ������ܺ�-����������ܺͣ���6��E��H-N��+3E��Cl-Cl��-6 E��H-Cl��-E��N��N��=-456kJ?mol-1����6��E��H-N��+3��243KJ/mol-6E��H-Cl��-945KJ/mol=-456kJ?mol-1�������õ�E��H-N��-E��H-Cl��=-40KJ/mol���Ͽ�1mol H-N����Ͽ�1mol H-Cl�������������ԼΪ40KJ������Խ��ѧ��Խ�ȶ�����NH3�е�H-N����HCl�е�H-Cl������
�ʴ�Ϊ��40kJ������
��4����װ��Ϊԭ��ط�Ӧ���������Һ���������������ƶ�����ͼ��֪������������b������֪aΪ������bΪ�����������ڵõ��������������ӣ�������ԭ��Ӧ��
�ʴ�Ϊ����ԭ��
��ʯīa�缫Ϊ����������ʧ���ӣ��������������ɵ�����ˮ���缫��ӦʽΪ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
���������⿼�������ƶϣ���Ŀ�Ƚ��ۺϣ��漰����ʽ��Ԫ�������ɡ����Ӽ��顢������ԭ��Ӧ���㡢�����뷴Ӧ�ʱ��ϵ����ѧ����������ԭ��صȣ���Ҫѧ���߱���ʵ�Ļ�����֪ʶǨ��Ӧ���������Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
������ʵ��������������ԭ�����͵��ǣ�������
| A����ҵ�������������ʹ�ù���������������߶��������ת���� |
| B���ϳɰ���ҵ�в��ø�ѹ |
| C��ʵ�������ű���ʳ��ˮ�ķ����ռ����� |
| D���Ӵ��������ںϳɰ��ķ�Ӧ |
ij������ȼ�ϵ�صĵ��ҺΪKOH��Һ�������йظõ�ص���������ȷ���ǣ�������
| A��������ӦʽΪ��O2+2H2O+4e-=4OH- |
| B������һ��ʱ����Һ��KOH�����ʵ������� |
| C����ȼ�ϵ�ص��ܷ�Ӧ����ʽΪ��2H2+O2=2H2O |
| D����������Դ��⾫��ͭʱ����ͭ�����������ڶƼ��ϵ��ͭʱ����ͭ������ |
 ij�¶��£���2L������3�����ʼ���з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ����Ӧ��t1minʱ����ƽ�⣬��ͼ��ʾ��
ij�¶��£���2L������3�����ʼ���з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ����Ӧ��t1minʱ����ƽ�⣬��ͼ��ʾ�� ij��ѧ�о���ѧϰС�������ȡ������̽�������ʵķ���������ͼ��ʾװ�����ʵ�飮��A�з�����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ���TMnCl2+Cl2��+2H2O��
ij��ѧ�о���ѧϰС�������ȡ������̽�������ʵķ���������ͼ��ʾװ�����ʵ�飮��A�з�����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ���TMnCl2+Cl2��+2H2O�� I��Fe2+��I-�����ֳ����Ļ�ԭ�����ӣ�
I��Fe2+��I-�����ֳ����Ļ�ԭ�����ӣ�