题目内容
下列物质中不属于电解质的是( )
| A、NaCl |
| B、CO2 |
| C、NaOH |
| D、BaSO4 |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答:
解:A.NaCl是化合物,在水溶液中或熔融状态下能够导电,属于电解质,故A不选;
B.二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,二氧化碳自身不能电离,二氧化碳是非电解质,故B可选;
C.NaOH是化合物,在水溶液中或熔融状态下能够导电,属于电解质,故C不选;
D.BaSO4是化合物,在熔融状态下能够导电,属于电解质,故D不选,
故选B.
B.二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,二氧化碳自身不能电离,二氧化碳是非电解质,故B可选;
C.NaOH是化合物,在水溶液中或熔融状态下能够导电,属于电解质,故C不选;
D.BaSO4是化合物,在熔融状态下能够导电,属于电解质,故D不选,
故选B.
点评:本题考查电解质、非电解质概念的辨析,难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.

练习册系列答案
相关题目
下面实验操作不能实现实验目的是( )
| A、鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加入水后沉淀溶解 |
| B、乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| C、取样灼烧,可以鉴别某白色纺织品是棉织品还是羊毛制品 |
| D、取少量淀粉溶液,加入一定量稀硫酸,水浴加热几分钟后,再加入新制的氢氧化铜悬浊液并且加热,观察现象,判断淀粉的水解的产物中是否含有葡萄糖 |
检验溶液中是否含有某种离子,下列操作方法正确的是( )
| A、向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- |
| B、向某溶液中加稀 HCl,无明显现象,再加入BaCl2 溶液产生白色沉淀,证明有SO42- |
| C、向某溶液中加入稀 HCl,放出能使澄清的石灰水变浑浊的气体,证明有CO32 |
| D、把H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,证明H2O2有还原性 |
下列事实不能用勒夏特列原理解释的是( )
| A、工业生产硫酸过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B、合成氨工业中采用高压 |
| C、实验室用排饱和食盐水的方法收集氯气 |
| D、加催化剂有利于合成氨的反应 |
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+5价
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定都为6
④周期表里主族元素所在的周期序数等于原子核外电子层数
⑤周期表里主族元素所在的族序数等于原子核外电子数
⑥元素周期表有7个主族,7个副族,1个0族,1个第Ⅷ族,共16纵行.
①原子序数为15的元素的最高化合价为+5价
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定都为6
④周期表里主族元素所在的周期序数等于原子核外电子层数
⑤周期表里主族元素所在的族序数等于原子核外电子数
⑥元素周期表有7个主族,7个副族,1个0族,1个第Ⅷ族,共16纵行.
| A、①②⑤ | B、②③⑥ |
| C、①②④ | D、②④⑤ |
有以下描述的事实:
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④在可逆反应中,使用催化剂有利于提高反应物的转化率;
⑤常温下,将1mol pH=3的醋酸溶液加水稀释至100ml,测得其pH<5
⑥二氧化氮与四氧化氮的平衡体系,加压后颜色加深.
其中能用勒夏特列原理解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④在可逆反应中,使用催化剂有利于提高反应物的转化率;
⑤常温下,将1mol pH=3的醋酸溶液加水稀释至100ml,测得其pH<5
⑥二氧化氮与四氧化氮的平衡体系,加压后颜色加深.
其中能用勒夏特列原理解释的是( )
| A、①②③ | B、④⑤⑥ |
| C、①③⑤ | D、①③④⑤ |
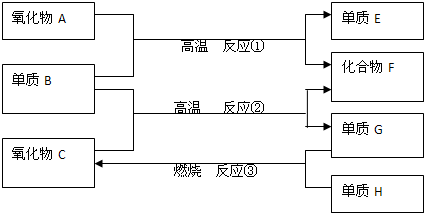
 I.Fe2+和I-是两种常见的还原性离子.
I.Fe2+和I-是两种常见的还原性离子.